VOCABRIA 600 mg SUSPENSION INYECTABLE DE LIBERACION PROLONGADA

Cómo usar VOCABRIA 600 mg SUSPENSION INYECTABLE DE LIBERACION PROLONGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Vocabria 600 mg suspensión inyectable de liberación prolongada
cabotegravir
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o enfermero.
- Si experimenta efectos adversos, consulte a su médico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Vocabria y para qué se utiliza
- Qué necesita saber antes de que le administren Vocabria
- Cómo se administra Vocabria inyectable
- Posibles efectos adversos
- Conservación de Vocabria
- Contenido del envase e información adicional
1. Qué es Vocabria y para qué se utiliza
Vocabria inyectable contiene cabotegravir como principio activo. Cabotegravir pertenece a un grupo de medicamentos antirretrovirales llamados inhibidores de la integrasa (INI).
Vocabria inyectable se usa para tratar la infección por el VIH (Virus de la Inmunodeficiencia Humana) en adultos y adolescentes (de al menos 12 años de edad y con un peso de al menos 35 kg), que también reciben otro medicamento antirretroviral inyectable llamado rilpivirina y cuya infección por el VIH-1 está bajo control.
Las inyecciones de Vocabria no curan la infección por el VIH; mantienen la cantidad de virus en su organismo en un nivel bajo. Esto ayuda a mantener el número de células CD4+ en la sangre. Las células CD4+ son un tipo de glóbulos blancos que son importantes para ayudar a su cuerpo a combatir las infecciones.
La inyección de Vocabria siempre se administraen combinación con otra inyección de otro medicamento antirretroviral llamado rilpivirina inyectable. Consulte el prospecto de rilpivirina para más información sobre ese medicamento.
2. Qué necesita saber antes de que le administren Vocabria
No reciba Vocabria inyectable
- si alguna vez ha desarrollado una erupción cutánea grave, descamación de la piel, ampollas y/o llagas en la boca.
- si es alérgico(hipersensible) a cabotegravir o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- si está tomando alguno de estos medicamentos ya que podrían afectar al modo en que Vocabria funciona:
- carbamazepina, oxcarbazepina, fenitoína, fenobarbital(medicamentos para tratar la epilepsia y prevenir las convulsiones)
- rifampicinao rifapentina(medicamentos para tratar algunas infecciones bacterianas, como la tuberculosis).
Si piensa que esto le afecta, informe a su médico.
Advertencias y precauciones
Reacción cutánea grave
Se han notificado muy raramente reacciones cutáneas graves, síndrome de Stevens-Johnson y necrólisis epidérmica tóxica, en asociación con Vocabria. Si nota alguno de los síntomas relacionados con estas reacciones cutáneas graves, no reciba la próxima inyección de Vocabria y busque atención médica inmediatamente.
Lea la informaciónde la sección 4 de este prospecto (“Posibles efectos adversos”).
Reacción alérgica
Vocabria contiene cabotegravir, que es un inhibidor de la integrasa. Los inhibidores de la integrasa, incluido cabotegravir, pueden causar una reacción alérgica grave conocida como reacción de hipersensibilidad. Necesita conocer cuáles son los signos y síntomas importantes a los que debe prestar atención mientras está recibiendo Vocabria.
Lea la informaciónen la sección 4 de este prospecto.
Problemas hepáticos que incluyen hepatitis B y/o C
Informe a su médico si tiene o ha tenido problemas hepáticos, incluyendo hepatitis B y/o C. Su médico evaluará la gravedad de su enfermedad del hígado antes de decidir si puede tomar Vocabria.
Esté atento a los síntomas importantes
Algunas personas que toman medicamentos para la infección por el VIH desarrollan otros trastornos, que pueden ser graves.
Necesita conocer los signos y síntomas importantes a los que debe prestar atención mientras está siendo tratado con Vocabria. Estos incluyen:
- síntomas de infección
- síntomas de daño hepático
Lea la informaciónen la sección 4 de este prospecto (“Posibles efectos adversos”).
Si usted tiene síntomas de infección o daño hepático:
Informe a su médico inmediatamente. No tome otros medicamentos para la infección si no se lo aconseja su médico.
Las visitas regulares son importantes
Es importante que asista a sus citas programadaspara recibir la inyección de Vocabria, para controlar su infección por VIH y evitar que su enfermedad empeore. Informe a su médico si está pensando en interrumpir el tratamiento. Si se retrasa en recibir su inyección de Vocabria, o si deja de recibir Vocabria, necesitará tomar otros medicamentos para tratar la infección por el VIH y para reducir el riesgo de desarrollar resistencia viral.
Vocabria inyectable es un medicamento de acción prolongada.Si interrumpe el tratamiento, niveles bajos de cabotegravir (el principio activo de Vocabria) pueden permanecer en su organismo hasta 12 meses o más tras la última inyección. Estos niveles bajos de cabotegravir no le protegerán frente al virus y el virus se puede volver resistente. Debe comenzar un tratamiento diferente frente al VIH en el plazo de un mes tras la última inyección de Vocabria, si está recibiendo inyecciones mensuales, y dentro de los dos meses posteriores a la última inyección de Vocabria, si recibe las inyecciones cada dos meses.
Niños y adolescentes
Este medicamento no se debe usar en niños menores de 12 años o adolescentes con un peso inferior a 35 kg, ya que no se ha estudiado en estos pacientes.
Otros medicamentos y Vocabria inyectable
Informe a su médico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento incluyendo otros medicamentos adquiridos sin receta.
Vocabria no se debe administrarcon otros medicamentos (ver ‘No reciba Vocabria inyectable’ anteriormente en la sección 2).
Algunos medicamentos pueden afectar al funcionamiento de Vocabriao aumentar la probabilidad de que sufra efectos adversos. Vocabria también puede afectar al modo en que otros medicamentos funcionan.
Informe a su médicosi usted está tomando:
- rifabutina(para tratar algunas infecciones bacterianas, como la tuberculosis).
Informe a su médicoo farmacéutico si está tomando este medicamento. Su médico puede decidir que necesita controles adicionales.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada:
Consulte a su médicoantes de recibir Vocabria inyectable.
Embarazo
- Vocabria no está recomendado durante el embarazo.Si es necesario, su médico considerará el beneficio para usted y el riesgo para su bebé de recibir inyecciones de Vocabria mientras está embarazada. Si está planeando quedarse embarazada, hable previamente con su médico.
- Si se ha quedado embarazada, no deje de asistir a sus citas para recibir la inyección de Vocabria sin consultar a su médico.
Lactancia
No se recomiendaque las mujeres que conviven con el VIH den el pecho porque la infección por VIH puede transmitirse al bebé a través de la leche materna.
Se desconocesi los componentes de Vocabria inyectable pueden pasar a la leche materna. Sin embargo, es posible que cabotegravir pudiera pasar a la leche materna durante los 12 meses siguientes a la última inyección de Vocabria.
Si está dando el pecho o piensa en dar el pecho, debe consultar con su médico lo antes posible.
Conducción y uso de máquinas
Vocabria puede hacer que se sienta mareadoy tener otros efectos adversos que le hagan estar menos atento.
No conduzca ni maneje maquinariaa menos que esté seguro de que no le afecta.
Información importante sobre algunos de los componentes de Vocabria
La inyección de Vocabria contiene polisorbato. Este medicamento contiene 60 mg de polisorbato por dosis de 3 ml. Informe a su médico si tiene alguna alergia conocida.
3. Cómo se administra Vocabria inyectable
Se le administrará Vocabria en forma de inyección, una vez al mes o una vez cada 2 meses, junto con otro medicamento inyectable llamado rilpivirina. Su médico le informará sobre la pauta de dosificación.
Un enfermero o médico le administrará Vocabria mediante una inyección en el músculo de su nalga (inyección intramuscular, o IM).
Cuando usted comience el tratamientocon Vocabria, usted y su médico pueden decidir iniciar el tratamiento con Vocabria comprimidos u optar directamente por las inyecciones de Vocabria. Si se decide iniciar el tratamiento con los comprimidos, su médico le dirá:
- que tome un comprimido de Vocabria 30 mg y un comprimido de rilpivirina 25 mg, una vez al día, durante aproximadamente un mes
- después, recibirá las inyeccionesde manera mensual o cada 2 meses.
Este primer mes de comprimidos de Vocabria y rilpivirina se denomina periodo de inducción oral.Permitirá a su médico evaluar si es apropiado pasar a las inyecciones.
Pauta de inyección mensual
Qué medicamento | Cuándo | |
Primera inyección | Segunda inyección en adelante, cada mes | |
Vocabria | Inyección de 600 mg | Inyección de 400 mg cada mes |
Rilpivirina | Inyección de 900 mg | Inyección de 600 mg cada mes |
Pauta de inyección cada 2 meses
Qué medicamento | Cuándo | |
Primera y segunda inyección, con un mes de diferencia | Tercera inyección en adelante, cada dos meses | |
Vocabria | Inyección de 600 mg | Inyección de 600 mg cada 2 meses |
Rilpivirina | Inyección de 900 mg | Inyección de 900 mg cada 2 meses |
Si omite una inyección de Vocabria
?Contacte con su médico inmediatamentepara programar una nueva cita
Es importante para controlar el VIH y evitar que su enfermedad empeore, que vaya a las citas programadas habituales para recibir su inyección. Hable con su médico si está pensando en interrumpir el tratamiento.
Hable con su médicosi piensa que no va a poder recibir su inyección de Vocabria con la frecuencia habitual. Su médico puede recomendarle que tome Vocabria comprimidos u otro tratamiento para el VIH en su lugar, hasta que pueda recibir su inyección de Vocabria de nuevo.
Si le administran más Vocabria inyectable del que debe
Este medicamento se lo administrará un médico o enfermero, por lo que es poco probable que le administren de más. Si está preocupado, consulte al médico o enfermero.
No deje de recibir inyecciones de Vocabria sin el consejo de su médico.
Continúe recibiendo inyecciones de Vocabria tanto tiempo como le recomiende su médico. No lo deje a menos que su médico se lo indique. Si interrumpe el tratamiento, su médico debe comenzar con otro tratamiento frente al VIH en el plazo de un mes tras la última inyección de Vocabria si está recibiendo inyecciones mensuales, y dentro de los dos meses posteriores a la última inyección de Vocabria si recibe las inyecciones cada dos meses, para reducir el riesgo de desarrollar resistencia viral.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
No reciba la próxima inyección de Vocabria y busque atención médica inmediatamentesi nota alguno de los siguientes síntomas:
- manchas rojizas no elevadas, en forma de diana o circulares en el tronco, a menudo con ampollas en el centro, descamación de la piel, llagas en la boca, garganta, nariz, genitales y ojos. Estas erupciones cutáneas graves pueden ir precedidas de fiebre y síntomas similares a los de la gripe (síndrome de Stevens-Johnson, necrólisis epidérmica tóxica). Estas reacciones cutáneas graves son muy raras (pueden afectar hasta 1 de cada 10000personas).
Reacciones alérgicas
Vocabria contiene cabotegravir, que es un inhibidor de la integrasa. Los inhibidores de la integrasa, incluido cabotegravir, pueden causar una reacción alérgica grave conocida como reacción de hipersensibilidad. Estas reacciones de hipersensibilidad son poco frecuentes (pueden afectar hasta 1 de cada 100personas).
Si padece alguno de los siguientes síntomas:
- reacción cutánea (erupción, habón)
- temperatura elevada (fiebre)
- falta de energía (fatiga)
- hinchazón, en ocasiones de la cara o boca (angioedema), que causa dificultad para respirar
- dolores musculares o articulares.
Acuda al médico de inmediato.Su médico puede considerar necesario realizar pruebas para controlar su hígado, riñones o sangre y puede que le indique que deje de tomar Vocabria.
Efectos adversos muy frecuentes
Estos pueden afectar a más de 1 de cada 10personas:
- dolor de cabeza
- reacciones en el lugar de inyección. En los estudios clínicos, la mayoría fueron generalmente de leves a moderadas y se volvieron menos frecuentes con el tiempo. Los síntomas pueden incluir:
- dolor (que en raras ocasiones puede incluir dificultad temporal al caminar) y malestar, una masa o bulto endurecido
- sensación de calor (pirexia), que puede ocurrir en la primera semana tras las inyecciones.
Efectos adversos frecuentes
Estos pueden afectar hasta 1 de cada 10personas:
- depresión
- ansiedad
- sueños anormales
- dificultad para dormir (insomnio)
- mareos
- náuseas
- vómitos
- dolor de estómago (dolor abdominal)
- gases (flatulencia)
- diarrea
- erupción
- dolor muscular (mialgia)
- falta de energía (fatiga)
- sensación de debilidad (astenia)
- malestar general
- aumento de peso.
- reacciones en el lugar de la inyección. En los estudios clínicos, la mayoría fueron generalmente de intensidad leve a moderada y se volvieron menos frecuentes con el tiempo. Los síntomas pueden incluir: enrojecimiento, picor, hinchazón, calor, hematomas (que pueden incluir decoloración o una acumulación de sangre debajo de la piel).
Efectos adversos poco frecuentes
Estos pueden afectar hasta 1 de cada 100personas:
- intento de suicidio y pensamientos suicidas (especialmente en pacientes que anteriormente han tenido depresión o problemas de salud mental)
- reacción alérgica (hipersensibilidad)
- habón (urticaria)
- hinchazón, en ocasiones de la cara o boca (angioedema), que causa dificultad para respirar
- sensación de somnolencia
- sensación de aturdimiento, durante o después de una inyección. Esto puede llevar a desmayos
- daño hepático (los signos pueden incluir coloración amarillenta de la piel y del blanco de los ojos, pérdida de apetito, picor, sensibilidad estomacal, heces de color claro u orina anormalmente oscura)
- cambios en marcadores hepáticos en los análisis de sangre (aumento de las transaminasaso aumento de la bilirrubina).
- reacciones en el lugar de la inyección. En los estudios clínicos, la mayoría fueron generalmente de intensidad leve a moderada y se volvieron menos frecuentes con el tiempo. Los síntomas pueden incluir: entumecimiento, sangrado leve, un absceso (acumulación de pus) o celulitis (calor, hinchazón o enrojecimiento).
Otros efectos adversos que pueden aparecer en análisis de sangre
- un incremento de lipasas (una sustancia producida por el páncreas).
Otros posibles efectos adversos
Las personas que reciben tratamiento frente al VIH con Vocabria y rilpivirina pueden tener otros efectos adversos.
Pancreatitis
Si tiene dolor intenso en el abdomen (barriga), esto puede deberse a una inflamación del páncreas (pancreatitis).
Informe a su médico,especialmente si el dolor se extiende y empeora.
Síntomas de infección e inflamación
Las personas con infección avanzada por el VIH (SIDA) tienen un sistema inmunitario debilitado y son más propensas a desarrollar infecciones graves (infecciones oportunistas). Cuando comienzan el tratamiento, el sistema inmunitario se fortalece, por lo que el cuerpo comienza a combatir estas infecciones.
Se pueden desarrollar síntomas de infección e inflamación, causados por:
- infecciones antiguas latentes que vuelven a aparecer a medida que el cuerpo las combate
- el sistema inmunológico ataca tejidos sanos (trastornos autoinmunes).
Los síntomas de los trastornos autoinmunes pueden aparecer muchos meses después de que empiece a tomar medicamentos para tratar la infección por el VIH.
Los síntomas pueden incluir:
- debilidad musculary/o dolor muscular
- doloro hinchazón de las articulaciones
- debilidadque comienza en las manos y los pies y asciende hacia el tronco del cuerpo
- palpitacioneso temblores
- hiperactividad(excesiva inquietud y movimiento).
Si tiene algún síntoma de infección:
Informe a su médico inmediatamente.No tome otros medicamentos para la infección sin consultar antes con su médico.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V.Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vocabria
Mantener este medicamento fuera de la vista y del alcance de los niños.
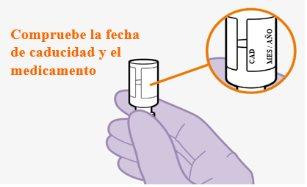
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y la caja después de CAD. La fecha de caducidad es el último día del mes que se indica.
No congelar.
6. Contenido del envase e información adicional
Composición de Vocabria
- El principio activo es cabotegravir.
Cada vial de 3 ml contiene 600 mg de cabotegravir.
Los demás componentes son:
Manitol (E421)
Polisorbato 20 (E432)
Macrogol (E1521)
Agua para preparaciones inyectables
Aspecto del producto y contenido del envase
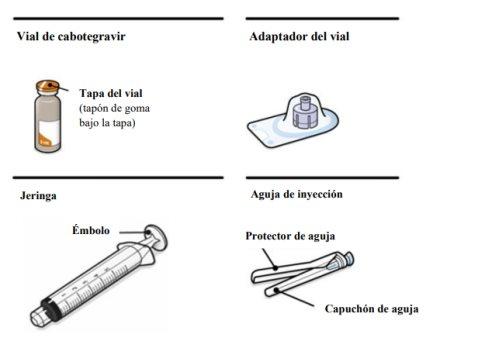
Cabotegravir suspensión inyectable de liberación prolongada se presenta en un vial de vidrio color topacio con tapón de goma. El envase también contiene 1 jeringa, 1 adaptador del vial y 1 aguja para la inyección.
Titular de la autorización de comercialización
ViiV Healthcare BV
Van Asch van Wijckstraat 55H
3811 LP Amersfoort
Países Bajos
Responsable de la fabricación
GlaxoSmithKline Manufacturing SpA
Strada Provinciale Asolana, 90
San Polo di Torrile
Parma, 43056
Italia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien ViiV Healthcare srl/bv Tél/Tel: + 32 (0) 10 85 65 00 | Lietuva ViiV Healthcare BV Tel: + 370 80000334 |
ViiV Healthcare BV Teπ.: + 359 80018205 | Luxembourg/Luxemburg ViiV Healthcare srl/bv Belgique/Belgien Tél/Tel: + 32 (0) 10 85 65 00 |
Ceská republika GlaxoSmithKline, s.r.o. Tel: + 420 222 001 111 | Magyarország ViiV Healthcare BV Tel.: + 36 80088309 |
Danmark GlaxoSmithKline Pharma A/S Tlf: + 45 36 35 91 00 | Malta ViiV Healthcare BV Tel: + 356 80065004 |
Deutschland ViiV Healthcare GmbH Tel.: + 49 (0)89 203 0038-10 | Nederland ViiV Healthcare BV Tel: + 31 (0) 33 2081199 |
Eesti ViiV Healthcare BV Tel: + 372 8002640 | Norge GlaxoSmithKline AS Tlf: + 47 22 70 20 00 |
Ελλáδα GlaxoSmithKline Μονοπρóσωπη A.E.B.E. Τηλ: + 30 210 68 82 100 | Österreich GlaxoSmithKline Pharma GmbH Tel: + 43 (0)1 97075 0 |
España Laboratorios ViiV Healthcare, S.L. Tel: + 34 900 923 501 | Polska GSK Services Sp. z o.o. Tel.: + 48 (0)22 576 9000 |
France ViiV Healthcare SAS Tél.: + 33 (0)1 39 17 69 69 | Portugal VIIVHIV HEALTHCARE, UNIPESSOAL, LDA Tel: + 351 21 094 08 01 |
Hrvatska ViiV Healthcare BV Tel: + 385 800787089 | România ViiV Healthcare BV Tel: + 40 800672524 |
Ireland GlaxoSmithKline (Ireland) Limited Tel: + 353 (0)1 4955000 | Slovenija ViiV Healthcare BV Tel: + 386 80688869 |
Ísland Vistor ehf. Sími: +354 535 7000 | Slovenská republika ViiV Healthcare BV Tel: + 421 800500589 |
Italia ViiV Healthcare S.r.l Tel: + 39 (0)45 7741600 | Suomi/Finland GlaxoSmithKline Oy Puh/Tel: + 358 (0)10 30 30 30 |
Κúπρος ViiV Healthcare BV Τηλ: + 357 80070017 | Sverige GlaxoSmithKline AB Tel: + 46 (0)8 638 93 00 |
Latvija ViiV Healthcare BV Tel: + 371 80205045 |
Fecha de la última revisión de este prospecto:<{MM/AAAA}.
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: https://www.ema.europa.eu
------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales sanitarios:
Instrucciones de usode Vocabria inyectable 3ml:
Descripción general Una dosis completa requiere dos inyecciones: VOCABRIA y rilpivirina 3 ml de cabotegravir y 3 ml de rilpivirina. Cabotegravir y rilpivirina son suspensiones que no requieren dilución ni reconstitución adicional. Los pasos para la preparación de ambos medicamentos son los mismos. Siga cuidadosamente estas instrucciones al preparar la suspensión inyectable para evitar fugas. Cabotegravir y rilpivirina son solo para uso intramuscular. Ambas inyecciones se deben administrar cada una en un glúteo. Nota:Se recomienda la zona ventroglútea. El orden de administración no es importante. | ||
Información de conservación | ||
| ||
Su envase contiene | ||
Tenga en cuenta la constitución del paciente y el criterio médico para elegir la longitud de aguja apropiada.
| ||
También necesitará | ||
Asegúrese de disponer del envase de rilpivirina antes de comenzar.
| ||
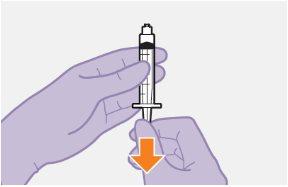
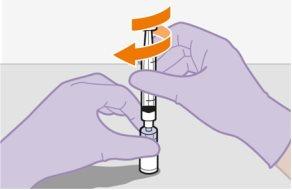
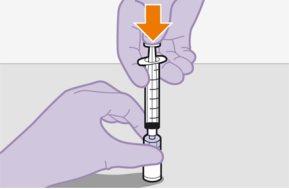
Preparación | ||
| ||
|
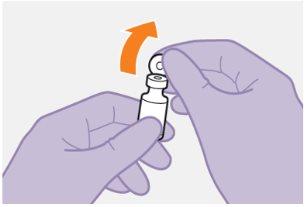
Nota:El vial de cabotegravir es de vidrio color topacio. No utilizarsi ha pasado la fecha de caducidad. | |
| ||
|
| |
| ||
|
| |
| ||
|
Nota:El orden de preparación de los viales no es importante. | |
| ||
|
| |
| ||
|
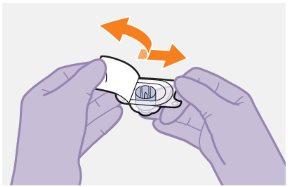
Nota:Noretire el adaptador de su embalaje hasta el siguiente paso. El adaptador nose caerá al darle la vuelta al embalaje. | |
| ||
|
| |
| ||
|
| |
| ||
|
| |
| ||
|
| |
| ||
|
| |
| ||
|
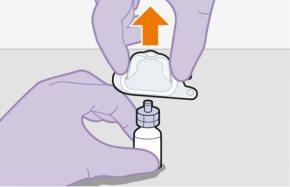
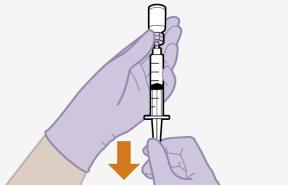
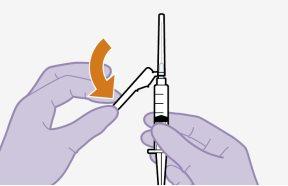
Nota:Mantenga la jeringa hacia arriba para evitar goteo. | |
| ||
|
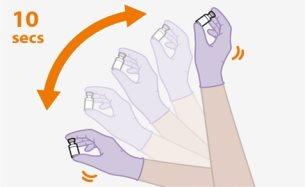
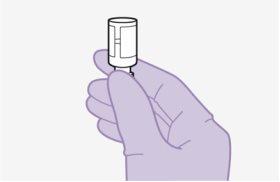
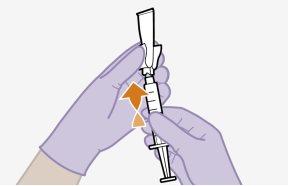
Nota:Compruebe que la suspensión de cabotegravir parece uniforme y de un color blanco a rosa claro. | |
| ||
|
| |
Inyección | ||
| ||
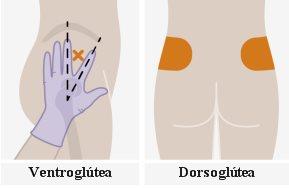
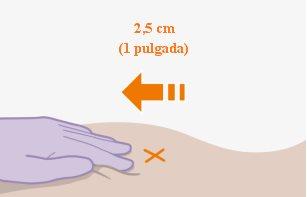
| Las inyecciones se deben administrar en los glúteos. Elija entre las siguientes zonas para la inyección:
Nota:Sólo para uso intramuscular glúteo.Nolo inyecte por vía intravenosa. | |
| ||
|
| |
| ||
|
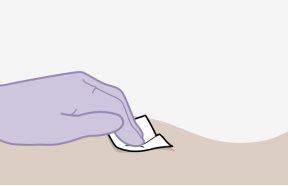
Nota:Limpie la zona de inyección con una toallita impregnada en alcohol. Deje que la piel se seque al aire antes de continuar. | |
| ||
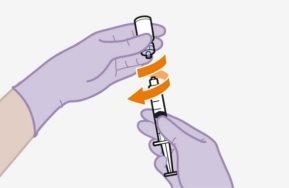
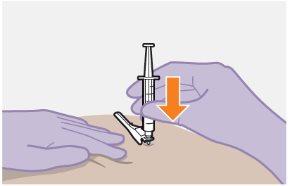
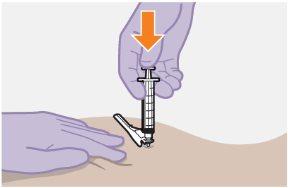
| Utilice la técnica de inyección en Z para minimizar el goteo de medicamento en el lugar de inyección.
| |
| ||
|
| |
| ||
|
| |
| ||
|
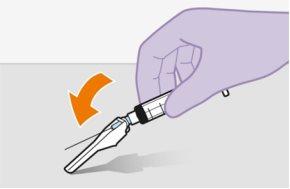
Nomasajee la zona. | |
| ||
|
| |
Tras la inyección | ||
| ||
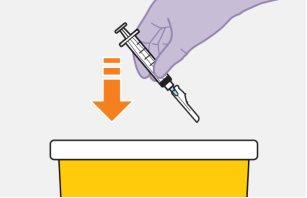
|
| |
Repita para el segundo medicamento | ||
| Si aún no ha inyectado ambos medicamentos, siga los pasos de preparación e inyección para la rilpivirina, que tiene sus propias instrucciones de uso. | |
Preguntas y respuestas | ||
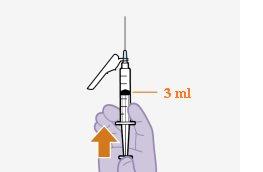
Una vez que la suspensión se ha cargado en la jeringa, la inyección debe utilizarse inmediatamente, desde un punto de vista microbiológico. Se ha demostrado estabilidad química y física en uso durante 2 horas a 25° C.
Inyectar 1 ml de aire en el vial facilita la extracción de la dosis con la jeringa. Sin el aire, parte del líquido puede retornar al vial sin querer, dejando menos de lo previsto en la jeringa.
No, el orden no es importante.
Lo mejor es dejar que el vial alcance la temperatura ambiente de manera natural. No obstante, puede usar el calor de sus manos para acelerar el tiempo de atemperación. No utilice ningún otro método de calentamiento. 5.¿Por qué se recomienda la administración en la zona ventroglútea? Se recomienda la administración en la zona ventroglútea, en el músculo glúteo medio, porque está más alejada de los principales nervios y vasos sanguíneos. También es aceptable la administración en la zona dorsoglútea, en el músculo glúteo mayor, si así lo prefiere el profesional sanitario. La inyección no se debe administrar en ninguna otra zona. |
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a VOCABRIA 600 mg SUSPENSION INYECTABLE DE LIBERACION PROLONGADAForma farmacéutica: COMPRIMIDO, 30 MGPrincipio activo: CabotegravirFabricante: Viiv Healthcare B.V.Requiere recetaForma farmacéutica: INYECTABLE, 600 MGPrincipio activo: CabotegravirFabricante: Viiv Healthcare B.V.Requiere recetaForma farmacéutica: COMPRIMIDO, 30 mgPrincipio activo: CabotegravirFabricante: Viiv Healthcare B.V.Requiere receta
Médicos online para VOCABRIA 600 mg SUSPENSION INYECTABLE DE LIBERACION PROLONGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de VOCABRIA 600 mg SUSPENSION INYECTABLE DE LIBERACION PROLONGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes