

Evertas

Consulta con un médico sobre la receta médica de Evertas

Cómo usar Evertas
Hoja de instrucciones del paquete: información para el usuario
Evertas, 4,6 mg/24 h, sistema transdérmico, parche
Evertas, 9,5 mg/24 h, sistema transdérmico, parche
Evertas, 13,3 mg/24 h, sistema transdérmico, parche
Rivastigmina
Es importante leer detenidamente el contenido de la hoja de instrucciones antes de utilizar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a su médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluyendo cualquier posible efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones
- 1. Qué es Evertas y para qué se utiliza
- 2. Información importante antes de utilizar Evertas
- 3. Cómo utilizar Evertas
- 4. Posibles efectos adversos
- 5. Cómo conservar Evertas
- 6. Contenido del paquete y otra información
1. Qué es Evertas y para qué se utiliza
El principio activo de Evertas es la rivastigmina.
La rivastigmina pertenece a un grupo de sustancias llamadas inhibidores de la colinesterasa. En pacientes
con demencia de tipo Alzheimer, se produce una disminución del número de células nerviosas
en el cerebro, lo que provoca una disminución de la concentración de acetilcolina, un neurotransmisor (sustancia que permite la comunicación entre las células nerviosas),
producida por ellas. El efecto de la rivastigmina consiste en bloquear las enzimas que causan la degradación de la acetilcolina:
acetilcolinesterasa y butirilcolinesterasa. Al bloquear el efecto de estas enzimas, la rivastigmina
permite aumentar la concentración de acetilcolina en el cerebro, lo que ayuda a aliviar los síntomas de la enfermedad de Alzheimer.
Evertas se utiliza para tratar a adultos con demencia de tipo Alzheimer leve a moderadamente grave,
una enfermedad cerebral progresiva que afecta gradualmente la memoria, las capacidades intelectuales y el comportamiento.
2. Información importante antes de utilizar Evertas
Cuándo no utilizar Evertas
- si el paciente es alérgico a la rivastigmina o a alguno de los demás componentes de este medicamento (enumerados en el punto 6);
- si el paciente tiene una reacción alérgica a medicamentos similares (derivados de la carbamida);
- si el paciente tiene una reacción cutánea que se extiende más allá del área de la piel cubierta por el parche, si se produce una reacción local grave (por ejemplo, ampollas, inflamación cutánea, hinchazón) y si estos cambios no desaparecen dentro de las 48 horas después de retirar el parche. Si esta situación se aplica al paciente, debe informar a su médico y no debe aplicar el parche de Evertas.
Precauciones y advertencias
Antes de comenzar a utilizar Evertas, debe discutir con su médico o farmacéutico si:
- el paciente tiene o ha tenido enfermedades cardíacas, como ritmo cardíaco irregular o lento, prolongación del intervalo QT, prolongación del intervalo QT en la familia, torsades de pointes, o niveles bajos de potasio o magnesio en la sangre;
- el paciente tiene o ha tenido úlcera gástrica activa;
- el paciente tiene o ha tenido dificultades para orinar;
- el paciente tiene o ha tenido convulsiones;
- el paciente tiene asma o enfermedad respiratoria grave;
- el paciente tiene temblor muscular;
- el paciente tiene un peso corporal bajo;
- el paciente tiene reacciones gastrointestinales, como náuseas (vómitos), vómitos y diarrea. El paciente puede deshidratarse (perder demasiado líquido) si los vómitos o la diarrea persisten durante un período prolongado;
- el paciente tiene trastornos hepáticos. Si alguna de estas situaciones se aplica al paciente, puede ser necesaria una observación más cercana por parte del médico durante el tratamiento con este medicamento.
Si el paciente no ha aplicado un parche durante más de tres días, no debe aplicar otro parche hasta que haya hablado con su médico.
Niños y adolescentes
No se recomienda utilizar Evertas en niños y adolescentes para tratar la demencia de tipo Alzheimer.
Evertas y otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar.
Evertas puede afectar la acción de los medicamentos anticolinérgicos, algunos de los cuales se utilizan para aliviar los espasmos gástricos (por ejemplo, dicicloverina), para tratar la enfermedad de Parkinson (por ejemplo, amantadina)
o para prevenir el mareo (por ejemplo, difenhidramina, escopolamina o meclizina).
No se debe utilizar el sistema transdérmico de Evertas, parche, al mismo tiempo que el metoclopramida (un medicamento utilizado para aliviar o prevenir las náuseas y los vómitos). La ingesta simultánea de estos dos medicamentos puede causar trastornos como rigidez de las extremidades y temblor de las manos.
Si el paciente va a someterse a una operación mientras está tomando Evertas, sistema transdérmico, parche, debe informar a su médico sobre su uso, ya que pueden aumentar el efecto de algunos relajantes musculares administrados durante la anestesia.
Debe tener cuidado al utilizar Evertas, sistema transdérmico, parche, con medicamentos beta-adrenolíticos (medicamentos como el atenolol, utilizados para tratar la hipertensión, el dolor en el pecho y otras enfermedades cardíacas). La ingesta simultánea de estos dos medicamentos puede causar trastornos como bradicardia (frecuencia cardíaca lenta) que puede llevar a la pérdida de conciencia o desmayo.
Debe tener cuidado al utilizar Evertas con otros medicamentos que puedan afectar el ritmo cardíaco o el sistema de conducción cardíaca (prolongación del intervalo QT).
Embarazo, lactancia y fertilidad
Si la paciente está embarazada o en período de lactancia, o si cree que puede estar embarazada o planea tener un hijo, debe consultar a su médico o farmacéutico antes de utilizar este medicamento.
Si la paciente está embarazada, se debe evaluar el beneficio del tratamiento con Evertas en relación con los posibles efectos del medicamento en el feto. Evertas no debe utilizarse durante el embarazo a menos que sea absolutamente necesario.
Durante el tratamiento con Evertas, sistema transdérmico, parche, no se debe amamantar.
Conducción de vehículos y uso de maquinaria
El médico informará al paciente si su condición le permite conducir vehículos o utilizar maquinaria. Evertas (parche) puede causar mareos o confusión severa. Si el paciente se siente débil o desorientado, no debe conducir vehículos, utilizar maquinaria ni realizar otras tareas que requieran concentración.
3. Cómo utilizar Evertas
Este medicamento siempre debe utilizarse exactamente como se describe en la hoja de instrucciones para el paciente, o según las indicaciones de su médico. En caso de dudas, debe consultar a su médico o farmacéutico.
ATENCIÓN:
- Antes de aplicar un nuevo parche, debe retirar el parche anterior.
- Debe aplicar solo UN parche de Evertas al día.
- No debe cortar el parche en trozos más pequeños.
- Debe presionar firmemente el parche con la palma de la mano durante al menos
30 segundos.
Cómo iniciar el tratamiento
El médico informará al paciente qué parches de Evertas son los mejores para su caso.
- El tratamiento generalmente comienza con Evertas 4,6 mg/24 h.
- La dosis diaria recomendada de Evertas es de 9,5 mg/24 h. Si el tratamiento es bien tolerado, el médico puede considerar aumentar la dosis a 13,3 mg/24 h
- Debe aplicar solo un parche de Evertas a la vez y cambiarlo cada 24 horas. Durante el tratamiento, el médico puede ajustar la dosis del medicamento según las necesidades del paciente.
Si el paciente no ha aplicado un parche durante más de tres días, no debe aplicar otro parche hasta que haya hablado con su médico. El tratamiento puede reanudarse con la misma dosis si la interrupción no ha superado los tres días. En caso contrario, el médico recomendará reanudar el tratamiento con una dosis de 4,6 mg/24 h de Evertas.
Evertas se puede utilizar con alimentos, bebidas y alcohol.
Dónde debe aplicar el parche de Evertas
- Antes de aplicar el parche, debe asegurarse de que la piel en el lugar de aplicación esté limpia, seca y sin vello, libre de polvo, aceites, cremas hidratantes o líquidos que puedan impedir la adhesión adecuada del parche, sin cortes, erupciones o irritaciones.
- Debe retirar con cuidado cualquier parche adherido antes de aplicar uno nuevo.La aplicación de varios parches en la piel puede exponer al paciente a una cantidad excesiva de medicamento, lo que puede ser peligroso.
- Debe aplicar UNparche al día en SOLO UNde los lugares posibles, como se muestra en los dibujos:
- parte superior del brazo izquierdo oparte superior del brazo derecho
- parte superior del pecho a la izquierda oa la derecha (evite aplicar parches en el pecho)
- parte superior de la espalda a la izquierda oa la derecha
- parte inferior de la espalda a la izquierda oa la derecha
Después de 24 horas, debe retirar el parche antiguo antes de aplicar UNparche nuevo en
SOLO UNde los lugares mostrados.
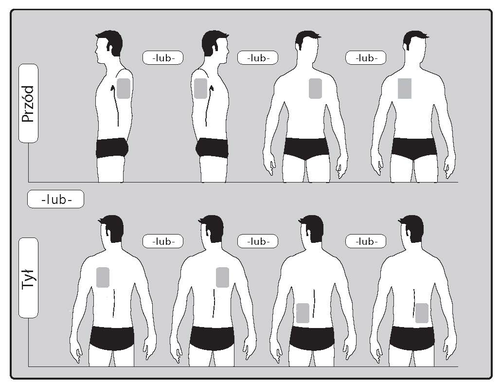
Al cambiar el parche, debe retirar el parche del día anterior antes de aplicar un nuevo parche en un lugar diferente (por ejemplo, un día en el lado derecho del cuerpo y al día siguiente en el lado izquierdo, un día en la parte superior del cuerpo y al día siguiente en la parte inferior). No debe aplicar un parche en el mismo lugar antes de que transcurran 14 días.
Cómo debe aplicar los parches de Evertas
Evertas es un parche delgado, de color marrón claro, hecho de plástico, que se adhiere a la piel. Cada parche se encuentra en una bolsa de protección sellada. No debe abrir la bolsa ni retirar el parche hasta el momento de aplicarlo en la piel.
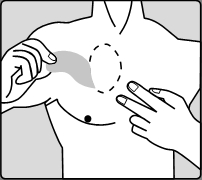
Debe retirar con cuidado el parche antes de aplicar uno nuevo.
Los pacientes que comienzan el tratamiento por primera vez y los pacientes que reanudan el tratamiento con rivastigmina después de una interrupción, deben
comenzar con las acciones mostradas en el segundo dibujo.
Cada parche se encuentra en una bolsa de protección sellada. La bolsa debe abrirse justo antes de utilizar el parche.
Debe cortar la bolsa en los dos lugares marcados con tijeras, pero no más allá de la línea indicada. Debe perforar la bolsa para abrirla. No debe cortar la bolsa a lo largo de toda su longitud para evitar dañar el parche.
Debe retirar el parche de la bolsa.
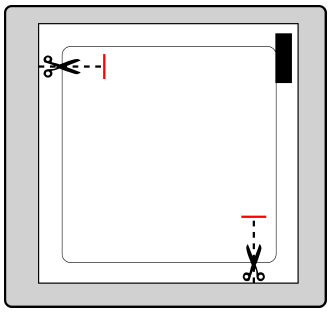
En el caso de los productos Evertas 4,6 mg/24 h y 9,5 mg/24h
sistema transdérmico, parche:
Debe retirar la cubierta de la parte superior, de color carne, del parche.
La parte adhesiva del parche está protegida por una capa de protección.
Debe retirar una parte de la capa de protección, sin tocar la parte adhesiva del parche.
En el caso del producto Evertas 13,3 mg/24 h sistema
transdérmico, parche:
La parte adhesiva del parche está protegida por una capa de protección.
Debe retirar una parte de la capa de protección, sin tocar la parte adhesiva del parche.
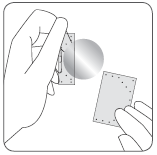
Debe aplicar la parte adhesiva del parche en la parte superior o inferior de la espalda, en la parte superior del brazo o en el pecho,
y luego retirar la segunda parte de la capa de protección.
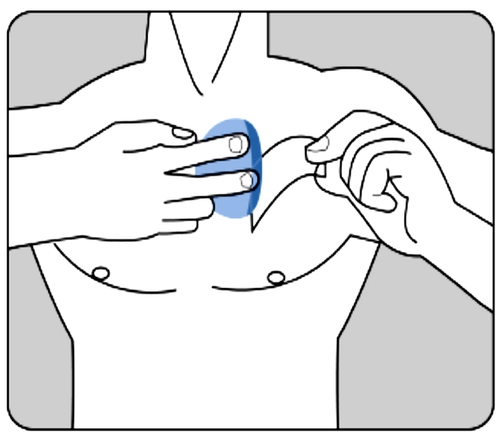
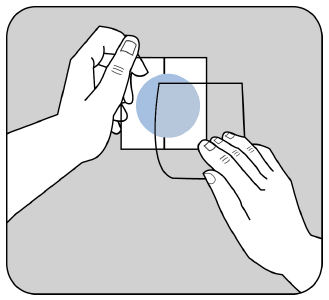
Debe presionar firmemente el parche con la palma de la mano durante al menos 30 segundos,
asegurándose de que los bordes se adhieran bien a la piel.
Puede firmar el parche con un bolígrafo, por ejemplo, con el nombre del día de la semana.
Debe llevar el parche constantemente, hasta que sea reemplazado por uno nuevo. El paciente puede probar diferentes lugares para aplicar el nuevo parche, para encontrar el más cómodo y menos propenso a ser arrancado por la ropa.
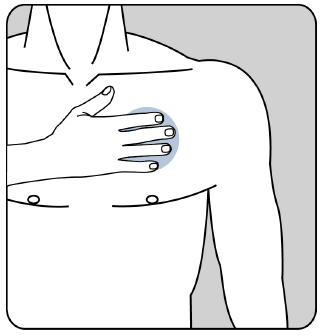
Cómo debe retirar el parche de Evertas
Debe tirar suavemente de un borde del parche y retirarlo lentamente de la piel. Si quedan restos de adhesivo en la piel, puede eliminarlos lavando la zona con agua tibia y jabón suave o aceite para bebés. No debe utilizar alcohol ni otros disolventes (quitaesmaltes y otros productos).
Después de retirar el parche, debe lavar sus manos con agua y jabón. En caso de contacto con los ojos o enrojecimiento ocular después del contacto con el parche, debe enjuagar los ojos con abundante agua y, si los síntomas no desaparecen, debe consultar a un médico.
Puede el paciente utilizar los parches de Evertas mientras se baña, nada o está al sol?
- El baño, la natación o la ducha no deben afectar la acción del parche. Debe asegurarse de que durante estas actividades no se suelte el parche.
- No debe exponer el parche a fuentes externas de calor durante períodos prolongados (por ejemplo, exposición excesiva a los rayos del sol, sauna, solárium).
Qué debe hacer el paciente si el parche se suelta?
Si el parche se suelta, debe aplicar uno nuevo para el resto del día y cambiarlo al día siguiente a la hora habitual.
Cuándo y durante cuánto tiempo debe el paciente utilizar los parches de Evertas?
- Para que el tratamiento sea efectivo, debe aplicar un nuevo parche cada día, preferiblemente a la misma hora cada día.
- Debe aplicar solo un parche de Evertas a la vez y cambiarlo cada 24 horas.
Uso de una dosis mayor de la recomendada de Evertas
Si el paciente aplica accidentalmente más de un parche, debe retirar todos los parches,
y luego informar a su médico sobre la aplicación accidental de más de un parche. El paciente puede necesitar atención médica. En algunas personas que han ingerido accidentalmente demasiada rivastigmina, se han producido náuseas, vómitos, diarrea, presión arterial alta y alucinaciones. También puede ocurrir una frecuencia cardíaca lenta y pérdida de conciencia.
Olvido de la aplicación de Evertas
Si el paciente se da cuenta de que ha olvidado aplicar un parche, debe hacerlo de inmediato. El siguiente parche se puede aplicar a la hora habitual del día siguiente. No debe aplicar dos parches para compensar la dosis olvidada.
Interrupción del tratamiento con Evertas
En caso de interrupción del tratamiento, debe informar a su médico o farmacéutico.
En caso de dudas adicionales sobre el uso de este medicamento, debe consultar a su médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Los efectos adversos se producen con más frecuencia durante el período inicial de tratamiento o durante el aumento de la dosis. Los efectos adversos generalmente desaparecen lentamente a medida que el organismo se adapta al tratamiento.
En caso de que se produzca alguno de los efectos adversos mencionados a continuación, debe retirar el parche y informar inmediatamente a su médico, ya que estos efectos pueden ser graves:
Frecuentes(se producen en menos de 1 de cada 10 pacientes):
- pérdida de apetito;
- mareos;
- agitación o somnolencia;
- incontinencia urinaria (incapacidad para retener la orina).
Poco frecuentes(se producen en menos de 1 de cada 100 pacientes):
- trastornos del ritmo cardíaco, como frecuencia cardíaca lenta;
- alucinaciones (ver cosas que no existen);
- úlcera gástrica;
- deshidratación (pérdida excesiva de líquido);
- agitación excesiva (nivel alto de actividad, agitación);
- agresividad.
Raros(se producen en menos de 1 de cada 1000 pacientes):
- caídas.
Muy raros(se producen en menos de 1 de cada 10 000 pacientes):
- rigidez de brazos o piernas;
- temblor de las manos.
Frecuencia no conocida(no puede determinarse a partir de los datos disponibles):
- reacción alérgica en el lugar de aplicación, como ampollas o inflamación cutánea;
- empeoramiento de los síntomas de la enfermedad de Parkinson, como temblor, rigidez o dificultad para caminar;
- pancreatitis - los síntomas incluyen un dolor abdominal superior severo, a menudo con náuseas (vómitos) o vómitos;
- frecuencia cardíaca rápida o irregular;
- presión arterial alta;
- convulsiones (ataques epilépticos);
- trastornos hepáticos (icoloración amarilla de la piel, ictericia ocular, orina oscura o náuseas, vómitos, fatiga y pérdida de apetito inexplicables);
- cambios en los resultados de las pruebas hepáticas;
- ansiedad,
- pesadillas,
- síndrome de Pisa (estado que incluye espasmo muscular involuntario con inclinación anormal del cuerpo y la cabeza hacia un lado).
En caso de que se produzca alguno de los efectos adversos mencionados a continuación, debe retirar el parche y informar inmediatamente a su médico.
Otros efectos adversos informados después de la administración de rivastigmina en forma de cápsulas o solución oral, que también pueden ocurrir con los parches:
Frecuentes(se producen en menos de 1 de cada 10 pacientes):
- salivación excesiva;
- pérdida de apetito;
- ansiedad;
- malestar general;
- temblor o confusión;
- sudoración excesiva.
Poco frecuentes(se producen en menos de 1 de cada 100 pacientes):
- trastornos del ritmo cardíaco (por ejemplo, frecuencia cardíaca rápida);
- dificultades para dormir;
- caídas accidentales.
Raros(se producen en menos de 1 de cada 1000 pacientes):
- convulsiones (ataques epilépticos);
- enfermedad ulcerosa intestinal;
- dolor en el pecho - puede ser causado por un espasmo cardíaco.
Muy raros(se producen en menos de 1 de cada 10 000 pacientes):
- presión arterial alta;
- pancreatitis - los síntomas incluyen un dolor abdominal superior severo, a menudo con náuseas (vómitos) o vómitos;
- hemorragias gastrointestinales - sangre en las heces o vómitos;
- alucinaciones (ver cosas que no existen);
- vómitos severos que pueden llevar a la ruptura de una parte del tracto gastrointestinal que conecta la boca con el estómago (esófago).
Información de efectos adversos
Si se producen efectos adversos, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Los efectos adversos pueden informarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad, Consumo y Bienestar Social, C/ Alcalá 56, 28071 Madrid, España. Teléfono: +34 91 596 34 00, fax: +34 91 596 34 01, sitio web: https://www.aemps.gob.es/
Los efectos adversos también pueden informarse al titular de la autorización de comercialización o a su representante en España.
5. Cómo conservar Evertas
Debe conservar este medicamento en un lugar que esté fuera del alcance de los niños.
No debe utilizar este medicamento después de la fecha de caducidad que se indica en el paquete y la bolsa después de "Caducidad (EXP)". La fecha de caducidad es el último día del mes indicado.
No hay instrucciones especiales para la conservación del medicamento.
Antes de su uso, el parche debe conservarse en la bolsa.
No debe utilizar un parche que esté dañado o que muestre signos de haber sido abierto.
Después de retirar el parche, debe doblarlo por la mitad con la parte adhesiva hacia adentro y presionarlo firmemente. Debe introducir el parche usado en la bolsa y luego tirarlo en un lugar inaccesible para los niños. Después de retirar el parche, no debe tocar los ojos con los dedos antes de lavar sus manos con agua y jabón.
No debe tirar los medicamentos por el desagüe ni por los contenedores de basura doméstica. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no necesita. Este comportamiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Evertas?
- El principio activo de Evertas es la rivastigmina. Evertas, 4,6 mg/24 h, sistema transdérmico: cada parche libera 4,6 mg de rivastigmina durante 24 horas. El parche tiene un área de 4,6 cm y contiene 6,9 mg de rivastigmina. Evertas, 9,5 mg/24 h, sistema transdérmico: cada parche libera 9,5 mg de rivastigmina durante 24 horas. El parche tiene un área de 9,2 cm y contiene 13,8 mg de rivastigmina. Evertas, 13,3 mg/24 h, sistema transdérmico: cada parche libera 13,3 mg de rivastigmina durante 24 horas. El parche tiene un área de 12,8 cm y contiene 19,2 mg de rivastigmina.
- Los demás componentes son:
Capa activa:
- Copolímero de acrilato de 2-etilhexilo y acetato de vinilo
Capa de matriz adhesiva:
- Poliisobutileno de masa molar media
- Poliisobutileno de masa molar alta
- Silicio dióxido coloidal anhidro
- Parafina líquida ligera
Capa exterior:
- Poliéster recubierto con poliéster/termoplástico/aluminio
Capa de protección (retirable):
- Poliéster recubierto con polímero fluorado
- Tinta naranja
Cómo se presenta Evertas y qué contiene el paquete?
Cada sistema transdérmico es un parche delgado y redondo hecho de plástico. En la capa exterior, de color marrón claro, hay una inscripción naranja que dice:
- “RIV-TDS 4.6 mg/24 h”
- “RIV-TDS 9.5 mg/24 h”
- “RIV-TDS 13.3 mg/24 h”
Cada parche se encuentra en una bolsa de protección sellada individual.
Evertas, 4,6 mg/24 h, sistema transdérmico
Evertas, 9,5 mg/24 h, sistema transdérmico
Los parches están disponibles en paquetes que contienen 7 o 30 sistemas transdérmicos, y en paquetes colectivos que contienen 60 (2x30) o 90 (3x30) sistemas transdérmicos.
Evertas, 13,3 mg/24 h, sistema transdérmico
Los parches están disponibles en paquetes que contienen 30 sistemas transdérmicos, y en paquetes colectivos que contienen 60 (2x30) o 90 (3x30) sistemas transdérmicos.
No todos los tamaños de paquete pueden estar disponibles en el mercado.
Titular de la autorización de comercialización
Zentiva, k.s., U kabelovny 130, Dolní Mĕcholupy, 102 37 Praga 10, República Checa
Fabricante
Luye Pharma AG, Am Windfeld 35, 83714 Miesbach, Alemania
S.C. Zentiva S.A, B-dul Theodor Pallady nr.50, sector 3, 032266 Bucarest, Rumania
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo bajo los siguientes nombres:
Polonia
Evertas
Rumania Evertas 4.6 mg/24 h plasture transdermic
Rumania Evertas 9.5 mg/24 h plasture transdermic
Para obtener más información sobre este medicamento, debe consultar al representante del titular de la autorización de comercialización en España:
Zentiva España, S.A.
C/ José Abascal 56, 4ª planta
28003 Madrid
Teléfono: +34 91 399 05 00
Fecha de la última revisión de la hoja de instrucciones:febrero 2025
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorLuye Pharma AG Zentiva SA
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a EvertasForma farmacéutica: Sistema, 4,6 mg/24 hPrincipio activo: RivastigminaFabricante: Luye Pharma AGRequiere recetaForma farmacéutica: Sistema, 9,5 mg/24 hPrincipio activo: RivastigminaFabricante: Luye Pharma AGRequiere recetaForma farmacéutica: Sistema, 4,6 mg/24 hPrincipio activo: RivastigminaRequiere receta
Alternativas a Evertas en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Evertas en Spain
Alternativa a Evertas en Ukraine
Médicos online para Evertas
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Evertas – sujeta a valoración médica y normativa local.











