

Гемосол Бо

Запитайте лікаря про рецепт на Гемосол Бо

Інструкція із застосування Гемосол Бо
Улотка до пакування: інформація для користувача
Hemosol B0 розчин для гемодіалізу/гемофілтрації
Хлорид натрію/хлорид кальцію дигідрат/хлорид магнію гексагідрат/молочна кислота/бікарбонат натрію
Перш ніж використовувати препарат, уважно ознайомтеся з вмістом улотки, оскільки вона містить важливу інформацію для пацієнта.
- Збережіть цю улотку, щоб у разі потреби ви могли її знову прочитати.
- Якщо у вас виникли будь-які сумніви, зверніться до лікаря, фармацевта або медсестри.
- Якщо в пацієнта виникли будь-які небажані симптоми, включаючи всі небажані симптоми, не перелічені в цій улотці, повідомте про це лікаря, фармацевта або медсестру. Див. пункт 4.
Зміст улотки
- 1. Що таке препарат Hemosol B0 і для чого він використовується
- 2. Інформація, важлива перед використанням препарату Hemosol B0
- 3. Як використовувати препарат Hemosol B0
- 4. Можливі небажані дії
- 5. Як зберігати препарат Hemosol B0
- 6. Зміст пакування та інші відомості
1. Що таке препарат Hemosol B0 і для чого він використовується
Препарат Hemosol B0 використовується в лікарнях на відділеннях інтенсивної терапії для корекції порушеної хімічної рівноваги крові, що виникла внаслідок ниркової недостатності. Лікування спрямоване на видалення з крові накопичених продуктів обміну речовин у осіб, чиї нирки не функціонують正常но.
Препарат Hemosol B0 використовується у дорослих і дітей будь-якого віку для наступних типів лікування:
- гемофілтрація,
- гемодіафільтрація та
- гемодіаліз.
2. Інформація, важлива перед використанням препарату Hemosol B0
Коли не використовувати препарат Hemosol B0:
Якщо пацієнт має алергію на одну з активних речовин або будь-яку з інших складових частини цього препарату (перелічених у пункті 6).
Попередження та заходи обережності
Перш ніж розпочати використання препарату Hemosol B0, обговоріть це з лікарем, фармацевтом або медсестрою.
Hemosol B0 є препаратом, який повинен використовуватися в лікарні і може бути введений лише кваліфікованими працівниками охорони здоров'я. Вони забезпечать безпечне використання препарату.
Перед лікуванням і під час його тривалості буде досліджуватися кров пацієнта, наприклад, контролюватиметься кислотно-лужна рівновага та концентрація солей (електролітів) у крові, а також усі рідини, введені (внутрішньовенне введення) і виведені (виділення сечі), навіть ті, які не мають прямого відношення до лікування.
Через те, що Hemosol B0 не містить калію, слід звернути особливу увагу на концентрацію калію у крові пацієнта. Якщо у пацієнта виявлено низьку концентрацію калію, може бути необхідне його доповнення.
Діти
Не існує спеціальних попереджень і заходів обережності щодо використання цього препарату у дітей.
Препарат Hemosol B0 та інші препарати
Повідомте лікаря або фармацевта про всі препарати, які приймає пацієнт зараз або останнім часом, а також про препарати, які пацієнт планує приймати, включаючи ті, які видаються без рецепта.
Під час лікування препаратом Hemosol B0 може зменшитися концентрація інших препаратів, які одночасно приймаються. Лікар, який проводить лікування, може порекомендувати зміну раніше прийманих препаратів.
Зокрема, слід повідомити лікаря, якщо пацієнт приймає будь-який з наступних препаратів:
- глікозиди серця (використовуються для лікування деяких серцевих захворювань), оскільки вони збільшують ризик нерегулярного або нападного ритму серця (розлади ритму серця), якщо концентрація калію у крові низька (гіпокаліємія);
- вітамін D і препарати, що містять кальцій, оскільки вони можуть збільшити ризик виникнення високої концентрації кальцію у крові (гіперкальціємія).
Додаткове введення бікарбонату натрію (або іншої буферної речовини) може збільшити ризик виникнення надміру бікарбонатів у крові (метаболічної алкалозу).
Якщо використовується цитрат як антикоагулянт, він може знижувати концентрацію кальцію в плазмі.
Вагітність, годування грудьми та вплив на фертильність
Якщо пацієнтка вагітна або годує грудьми, підозрює, що може бути вагітна або планує мати дитину, вона повинна проконсультуватися з лікарем або фармацевтом перед використанням цього препарату. Не передбачається впливу препарату на фертильність, вагітність чи на новонароджених/дітей, яких годують грудьми. Лікар, який проводить лікування, повинен зважити співвідношення користі та ризику перед введенням препарату Hemosol B0 пацієнтці під час вагітності або годування грудьми.
Керування транспортними засобами та обслуговування машин
Hemosol B0 не впливає на здатність керувати транспортними засобами та обслуговувати машини.
3. Як використовувати препарат Hemosol B0
Hemosol B0 є препаратом, який повинен використовуватися в лікарні і може бути введений лише кваліфікованими працівниками охорони здоров'я.
Об'єм препарату Hemosol B0, тобто введена доза, залежить від клінічного стану пацієнта. Доза (об'єм) буде визначена лікарем, відповідальним за лікування.
Hemosol B0 може бути введений безпосередньо в кровотік (внутрішньовенно) або через гемодіаліз, під час якого розчин проходить з однієї сторони діалізної мембрани, а кров - з іншої.
Введення більшої, ніж рекомендована, дози препарату Hemosol B0
Hemosol B0 є препаратом, який повинен використовуватися в лікарні і може бути введений лише кваліфікованими працівниками охорони здоров'я, а рівновага рідин, електролітів та кислотно-лужна рівновага буде уважно контролюватися у пацієнта.
У зв'язку з цим, дуже малоймовірно, щоб пацієнт отримав більшу дозу препарату Hemosol B0, ніж рекомендована.
Однак, якщо відбулося передозування, лікар, який проводить лікування, прийме необхідні заходи та调整є дозу.
Передозування може привести до:
- зbyt великої кількості рідини у крові,
- збільшення концентрації бікарбонату у крові (метаболічна алкалоз)
- і (або) зменшення концентрації солей у крові (гіпофосфатемія, гіпокаліємія).
Для ознайомлення з інструкцією щодо використання препарату див. пункт «Інформація, призначена лише для фахівців медичного персоналу».
Якщо у вас виникли будь-які подальші сумніви щодо використання цього препарату, зверніться до лікаря, фармацевта або медсестри.
4. Можливі небажані дії
Як і будь-який препарат, цей препарат може спричиняти небажані дії, хоча не у кожного вони виникнуть.
Згідно з даними, були зареєстровані наступні небажані дії:
Частота: невідома (частота не може бути визначена на основі наявних даних)
- зміни концентрації мінеральних солей у крові (розлади електролітної рівноваги, такі як гіпофосфатемія, гіпокаліємія);
- збільшення концентрації бікарбонату в плазмі (метаболічна алкалоз) або зменшення концентрації бікарбонату в плазмі (метаболічна ацидоз);
- неправильна велика або мала кількість води в організмі (перегідратування або деґідратування);
- нудота;
- воміт;
- спазми м'язів;
- низький тиск крові (гіпотонія).
Звітність про небажані дії
Якщо виникли будь-які небажані симптоми, включаючи всі небажані симптоми, не перелічені в цій улотці, повідомте про це лікаря, фармацевта або медсестру. Про небажані дії можна повідомляти безпосередньо до Департаменту моніторингу небажаних дій лікарських засобів Міністерства охорони здоров'я України
вул. Миколи Амосова, 7
03022, м. Київ
Телефон: +38 (044) 279-64-04
Факс: +38 (044) 279-64-04
Веб-сайт: https://smz.ezdrowie.gov.pl
Про небажані дії можна повідомляти також відповідальній особі.
Звітність про небажані дії дозволить зібрати більше інформації про безпеку використання препарату.
5. Як зберігати препарат Hemosol B0
Препарат слід зберігати в місці, недоступному для дітей.
Не використовувати цей препарат після закінчення терміну придатності, вказаного на зворотному боці мішка та на етикетці коробки після: Термін придатності. Термін придатності означає останній день вказаного місяця.
Не слід зберігати при температурі нижче 4°C.
Встановлено, що готовий до використання розчин зберігає хімічну та фізичну стабільність протягом 24 годин при температурі 22°C. З мікробіологічної точки зору, готовий до використання розчин слід застосовувати негайно. Якщо він не буде негайно використаний, відповідальність за час і умови зберігання такого розчину перед застосуванням лежить на користувачі, а час зберігання не повинен бути довшим за 24 години, включаючи час лікування.
Лікарських засобів не слід викидати у каналізацію чи домашні контейнери для відходів. Слід запитати фармацевта, як усунути лікарські засоби, яких більше не використовують. Таке поводження допоможе захистити навколишнє середовище.
6. Зміст пакування та інші відомості
Що містить препарат Hemosol B0
Активні речовини перед змішуванням та після змішування наведені нижче.
Активні речовини перед змішуванням:
1000 мл розчину, що міститься у малій камері (А), містить:
Хлорид кальцію, 2Н2О
5,145 г
Хлорид магнію, 6Н2О
2,033 г
Молочна кислота
5,4 г
1000 мл розчину, що міститься у великій камері (Б), містить:
Бікарбонат натрію
3,09 г
Хлорид натрію
6,45 г
Активні речовини після змішування:
Склад розчину (5000 мл) після змішування вмісту камери А (250 мл) та камери Б (4750 мл) такий:
ммоль/л
Кальцій, Ca
1,75
Магній, Mg
0,5
Натрій, Na
140
Хлориди, Cl
109,5
Молочаті
3
Бікарбонати, HCO3
32
Теоретична осмоларність: 287 мОсм/л
Інші складові:діоксид вуглецю (Е 290) та вода для ін'єкцій.
Як виглядає препарат Hemosol B0 та що містить пакування
Hemosol B0 міститься у двокамерному мішку. Мішок поміщений у прозоре зовнішнє пакування.
Для отримання готового до використання розчину слід розламати розривний шов та змішати обидва розчини.
Готовий до використання розчин прозорий та безбарвний. Кожен мішок (А+Б) містить 5000 мл розчину для гемофілтрації, гемодіафільтрації та (або) гемодіалізу.
Кожна коробка містить два мішки та одну улотку для пацієнта.
Відповідальна особа
Vantive Belgium SRL
Бульвар д'Англетер, 2
1420 Брен-л'Аллуд
Бельгія
Виробник
Bieffe Medital S.p.A.,
Віа Стельвіо, 94,
23035 Сондальо (СО),
Італія
або
Vantive Manufacturing Limited,
Монін Роуд,
Каслбар,
Графство Мейо
F23 XR63
Ірландія
Цей лікарський засіб дозволений до обігу в країнах-членах Європейського економічного простору та у Великій Британії (Північній Ірландії) під наступними назвами:
Австрія, Бельгія, Болгарія, Хорватія, Кіпр, Чехія, Данія, Естонія, Фінляндія, Франція, Німеччина,
Греція, Ісландія, Ірландія, Латвія, Литва, Люксембург, Мальта, Нідерланди, Норвегія, Польща, Португалія,
Словаччина, Словенія, Іспанія, Швеція, Велика Британія (Північна Ірландія): Hemosol B0.
Дата останньої актуалізації улотки: вересень 2024 -------------------------------------------------------------------------------------------------------------------------
Інформація, призначена лише для фахівців медичного персоналу
Hemosol B0 розчин для гемодіалізу/гемофілтрації
Заходи обережності
Слід суворо дотримуватися інструкції щодо використання/поведінки з лікарським засобом Hemosol B0.
Розчини з обох камер повиннібути змішані до використання.
Застосування забрудненого розчину для гемофілтрації може спричинити сепсис, шок та смерть пацієнта.
Для підвищення комфорту пацієнта Hemosol B0 можна підігріти до температури 37°C. Підігрівання розчину перед використанням слід виконувати до відновлення та виключно з використанням сухого джерела тепла. Розчинів не слід підігрівати у водяній лазні чи мікрохвильовій печі. Якщо розчин та пакування дозволяють, перед введенням слід контролювати візуально розчин для виявлення наявності твердих частинок та зміни забарвлення. Не вводіть, якщо розчин не є прозорим або шов пошкоджений.
Додаткове введення бікарбонату натрію може збільшити ризик виникнення метаболічної алкалозу.
Перед початком лікування та під час його тривалості слід суворо контролювати рівновагу електролітів та кислотно-лужну рівновагу. Через те, що Hemosol B0 не містить калію, концентрація калію в сироватці повинна бути контролювана перед та під час гемофілтрації та (або) гемодіалізу.
Може бути необхідне доповнення калію.
До розчину можна додати фосфати у кількості до 1,2 ммоль/л. При додаванні фосфату калію загальна концентрація калію не повинна перевищувати 4 мЕк/л (4 ммоль/л).
Об'єм та швидкість, з якою використовується лікарський засіб Hemosol B0, залежать від концентрації електролітів у крові, кислотно-лужної рівноваги та загального клінічного стану пацієнта.
Спосіб введення (дозу, швидкість інфузії та загальний об'єм) лікарського засобу Hemosol B0 повинен бути визначений лікарем. Континуюча гемофілтрація видаляє надмірну рідину та електроліти.
Якщо виникне порушення рівноваги рідин, слід суворо контролювати клінічний стан пацієнта та за необхідності коригувати рівновагу рідин.
Якщо пацієнт страждає на ниркову недостатність, унаслідок передозування може виникнути перевантаження рідинами та можуть виникнути серйозні наслідки, такі як застійна ниркова недостатність, порушення електролітного або кислотно-лужного балансу.
Через те, що розчин не містить глюкози, його введення може спричинити виникнення гіпоглікемії.
Слід регулярно контролювати концентрацію глюкози у крові.
Hemosol B0 містить бікарбонат (двухвуглецеву кислоту) та молочну кислоту (попередник бікарбонату), які можуть впливати на кислотно-лужну рівновагу пацієнта. Якщо під час лікування з використанням розчину виникне або погіршиться метаболічна алкалоз, може виникнути необхідність зменшення швидкості введення або припинення введення лікарського засобу.
Дозування
Загально прийнята швидкість потоку заміщення розчину у гемофілтрації та гемодіафільтрації становить:
Дорослі:
500-3000 мл/год.
Загально прийнята швидкість потоку діалізного розчину (діалізату) у континуючому гемодіалізі становить:
Дорослі:
500-2500 мл/год.
У дорослих зазвичай використовується загальна швидкість потоку, яка становить від близько 2000 до 2500 мл/год, що відповідає добовому об'єму рідини, який міститься в межах від близько 48 до 60 л.
Діти та підлітки
Діапазон швидкості потоку заміщення розчину у гемофілтрації та гемодіафільтрації та діалізного розчину (діалізату) у континуючому гемодіалізі становить:
Діти (від новонароджених до підлітків до 18 років): 1000-2000 мл/год/1,73 м².
Потрібна швидкість потоку може становити до 4000 мл/год/1,73 м², особливо у молодших дітей (≤10 кг). Безумовна швидкість потоку (у мл/год) у дітей та підлітків зазвичай не повинна перевищувати максимальну швидкість потоку, яка використовується у дорослих.
Інструкція щодо використання/поведінки
Для отримання готового до використання розчину розчин електролітів (мала камера А) слід додати до розчину буферної речовини (велика камера Б) після розламування розривного шва безпосередньо перед використанням.
Використовуйте виключно з відповідним обладнанням для позаорганного лікування ниркової недостатності.
Під час проведення та введення лікарського засобу пацієнту слід використовувати асептичну техніку.
Використовуйте виключно тоді, коли зовнішнє захисне пакування не пошкоджене, всі шви не порушені, розривний шов не пошкоджений, а розчин прозорий. Сильно стисніть мішок, щоб перевірити його цілісність. У разі виявлення витоку розчин слід негайно викинути, оскільки не можна гарантувати стерильність.
Велика камера Б оснащена портом для ін'єкцій, який дозволяє після відновлення розчину додати інші необхідні лікарські засоби. Лікар відповідає за оцінку сумісності додаткового лікарського засобу з препаратом Hemosol B0 шляхом перевірки, чи не виникають зміни кольору та (або) утворення осаду, появи неріворозчинних комплексів або кристалів. Перед додаванням лікарського засобу слід перевірити, чи він розчиняється та стабільний у воді з pH, рівним pH препарату Hemosol B0 (pH готового до використання розчину становить 7,0-8,5). Додаткові складові можуть не бути сумісними з розчином. Слід ознайомитися з інструкцією щодо використання додаваного лікарського засобу.
Слід видалити рідину з порту для ін'єкцій, тримати мішок дном догори, введіть лікарський засіб у порт для ін'єкцій та повністю перемішайте. Слід негайно розпочати введення розчину.
Введення та перемішування додаткових складових завжди повинні бути виконані перед підключенням мішка з розчином до позаорганного обводу.
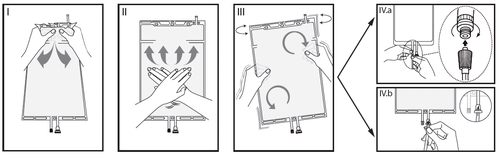
I
Безпосередньо перед використанням видаліть зовнішнє пакування з мішка та викиньте всі інші матеріали пакування. Відкрийте захисний механізм, розламавши розривний шов, розташований між двома камерами мішка. Розривний шов залишається у мішку.
(Див. рисунок I нижче).
II
Переконайтеся, що весь рідина з малої камери А був перекачаний у велику камеру Б. (Див. рисунок II нижче).
III
Прополоскайте двічімалу камеру А, виштовхуючи змішаний розчин назад у малу камеру А, а потім знову у велику камеру Б. (Див. рисунок III нижче).
IV
Якщо мала камера А порожня: потрясайте велику камеру Б для повного перемішування її вмісту. Тепер розчин готовий до використання, і мішок можна підвісити на стійку. (Див. рисунок IV нижче).
V
До кожного з двох портів доступу можна підключити лінію діалізу або обміну.
V.a
Якщо використовується доступ типу луер, видаліть затичку та підключіть чоловічий конектор типу луер лока лінії діалізу або обміну до жіночого конектора типу луер рецептора на мішку; затисніть.
Тримаючи великим та вказівним пальцями, розламайте кольоровий розривний шов у його основі та рухайте його назад та вперед. Не використовуйте інструменти. Переконайтеся, що затичка повністю розділена та що рідина протікає вільно. Під час лікування затичка залишається у порті типу луер.
(Див. рисунок V.a нижче).
V.bЯкщо використовується порт для ін'єкцій, спочатку видаліть затичку шляхом її розламування. Порт для ін'єкцій можна протирати дезинфікуючими засобами. Потім проколіть голкою гумову перегородку. Переконайтеся, що рідина протікає вільно. (Див. рисунок V.b нижче).
Готовий до використання розчин слід застосовувати негайно після видалення зовнішнього пакування.
Якщо готовий до використання розчин не буде негайно застосований, його слід використати протягом 24 годин, включаючи час лікування, після додавання розчину електролітів до розчину буферної речовини.
Готовий до використання розчин призначений виключно для одноразового використання. Слід викинути невикористаний розчин негайно після застосування.
Всі невикористані залишки лікарського засобу або його відходи слід видалити згідно з місцевими правилами.
1. Що таке препарат Гемосол Б0 і для чого він застосовується
Препарат Гемосол Б0 застосовується в лікарнях на відділеннях інтенсивної терапії з метою виправлення
порушеної хімічної рівноваги крові, що виникла внаслідок ниркової недостатності. Лікування спрямоване
на видалення з крові нагромаджених продуктів обміну речовин у осіб, чиї нирки не функціонують
правильно.
Препарат Гемосол Б0 застосовується у дорослих і дітей будь-якого віку при наступних типах лікування:
- гемофільтрація,
- гемодіафільтрація та
- гемодіаліз.
2. Важлива інформація перед застосуванням препарату Гемосол Б0
Коли не застосовувати препарат Гемосол Б0:
Якщо у пацієнта є алергія на одну з активних речовин або будь-яку з інших складових частини цього препарату (перелічених у пункті 6).
Остережності та заходи обережності
Перед початком застосування препарату Гемосол Б0 необхідно обговорити це з лікарем, фармацевтом або
медсестрою.
Гемосол Б0 є препаратом, який необхідно застосовувати в лікарні і може бути введений лише професійними працівниками охорони здоров'я. Вони забезпечать безпечне застосування препарату.
Перед лікуванням і під час його тривалості буде досліджуватися кров пацієнта, наприклад, контролюватися кислотно-лужна рівновага та концентрація солей (електролітів) у крові, а також всі рідини, введені (внутрішньовенне введення) і видалені (виділення сечі), навіть ті, які не пов'язані безпосередньо з лікуванням.
Через те, що Гемосол Б0 не містить калію, необхідно звернути особливу увагу на концентрацію калію у крові пацієнта. Якщо у пацієнта виявлено низьку концентрацію калію, може знадобитися його доповнення.
Діти
Не існує спеціальних попереджень і заходів обережності щодо застосування цього препарату у дітей.
Препарат Гемосол Б0 та інші препарати
Необхідно повідомити лікаря або фармацевта про всі препарати, які приймає пацієнт зараз або останнім часом, а також про препарати, які пацієнт планує приймати, включаючи ті, які видавляються без рецепта.
Під час лікування препаратом Гемосол Б0 може зменшитися концентрація інших препаратів, які застосовуються одночасно. Лікар, який проводить лікування, може рекомендувати зміну раніше застосовуваних препаратів.
Особливо необхідно повідомити лікаря, якщо пацієнт приймає будь-який з наступних препаратів:
- глікозиди серця (застосовуються при лікуванні деяких серцевих захворювань), оскільки вони збільшують ризик нерегулярного або нападного ритму серця (порушення ритму серця), якщо концентрація калію у крові низька (гіпокаліємія);
- вітамін Д і препарати, які містять кальцій, оскільки вони можуть збільшити ризик розвитку високої концентрації кальцію у крові (гіперкальціємія).
Додаток бікарбонату натрію (або іншої буферної речовини) може збільшити ризик розвитку надміру бікарбонатів у крові (метаболічна алкалоз).
Якщо застосовується цитрат як антикоагулянт, він може знижувати концентрацію кальцію в плазмі.
Вагітність, годування грудьми та вплив на фертильність
Якщо пацієнтка вагітна або годує грудьми, припускає, що може бути вагітна або планує мати
дитину, вона повинна проконсультуватися з лікарем або фармацевтом перед застосуванням цього препарату. Не передбачається вплив препарату на фертильність, вагітність чи на новонароджених/дітей, яких годують грудьми. Лікар, який проводить лікування, повинен зважити співвідношення користі та ризику перед введенням препарату Гемосол Б0 пацієнтці, яка вагітна або годує грудьми.
Керування транспортними засобами та обслуговування машин
Препарат Гемосол Б0 не впливає на здатність керувати транспортними засобами та обслуговувати машини.
3. Як застосовувати препарат Гемосол Б0
Препарат Гемосол Б0 є препаратом, який необхідно застосовувати в лікарні і може бути введений лише професійними працівниками охорони здоров'я.
Об'єм препарату Гемосол Б0, тобто застосована доза, залежить від клінічного стану пацієнта. Доза (об'єм) буде визначена лікарем, який проводить лікування.
Препарат Гемосол Б0 може бути введений безпосередньо в кровотік (внутрішньовенно) або через гемодіаліз, під час якого розчин проходить з однієї сторони діалізної мембрани, а кров - з іншої.
Застосування більшої, ніж рекомендована, дози препарату Гемосол Б0
Препарат Гемосол Б0 є препаратом, який необхідно застосовувати в лікарні і може бути введений лише професійними працівниками охорони здоров'я, а рівновага рідин, електролітів та кислотно-лужна рівновага буде уважно контролюватися у пацієнта.
У зв'язку з цим, дуже малоймовірно, щоб пацієнт отримав більшу дозу препарату Гемосол Б0, ніж рекомендована.
Препарат Гемосол Б0
Однак, якщо доjde до передозування, лікар, який проводить лікування, прийме необхідні заходи та відкоригує дозу.
Передозування може привести до:
- зbyt великої кількості рідини у крові,
- збільшення концентрації бікарбонатів у крові (метаболічна алкалоз)
- і (або) зниження концентрації солей у крові (гіпофосфатемія, гіпокаліємія).
Для ознайомлення з інструкцією щодо застосування препарату див. пункт «Інформація, призначена лише для фахівців охорони здоров'я».
У разі будь-яких подальших сумнівів, пов'язаних з застосуванням цього препарату, необхідно звернутися до лікаря, фармацевта або медсестри.
4. Можливі побічні ефекти
Як і будь-який препарат, цей препарат може спричиняти побічні ефекти, хоча не у всіх вони виникнуть.
Згідно з даними, були зареєстровані наступні побічні ефекти:
Частота: невідома (частота не може бути визначена на основі доступних даних)
- зміни концентрації мінеральних солей у крові (порушення електролітної рівноваги, такі як гіпофосфатемія, гіпокаліємія);
- збільшення концентрації бікарбонатів у плазмі (метаболічна алкалоз) або зниження концентрації бікарбонатів у плазмі (метаболічна ацидоз);
- неправильна велика або мала кількість води в організмі (перегідратування або деґідратування);
- нудота;
- воміта;
- спазми м'язів;
- низький тиск крові (гіпотонія).
Зголошення побічних ефектів
Якщо виникнуть будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перераховані у вкладиші, необхідно повідомити про це лікаря, фармацевта або медсестру. Побічні ефекти можна zgолошувати безпосередньо до Департаменту моніторингу побічних ефектів лікарських засобів Міністерства охорони здоров'я
вул. Європейська, 2
02000 м. Київ
Телефон: +38 (044) 279-64-04
Факс: +38 (044) 279-64-04
Веб-сайт: https://www.moz.gov.ua
Побічні ефекти також можна zgолошувати відповідальному суб'єкту.
Зголошення побічних ефектів дозволить зібрати більше інформації про безпеку застосування препарату.
5. Як зберігати препарат Гемосол Б0
Препарат необхідно зберігати в місці, недоступному для дітей.
Не застосовувати цей препарат після закінчення терміну придатності, зазначеного на зворотній стороні мішка та на етикетці коробки: Термін придатності. Термін придатності позначає останній день вказаного місяця.
Не зберігати при температурі нижче 4°C.
Встановлено, що готовий до застосування розчин зберігає хімічну та фізичну стабільність протягом 24 годин при температурі 22°C. З мікробіологічної точки зору, готовий до застосування розчин необхідно застосувати негайно. Якщо він не буде негайно застосований, відповідальність за час та умови зберігання такого розчину перед застосуванням лежить на користувачі, а час зберігання не повинен перевищувати 24 години, включаючи час лікування.
Лікарських засобів не слід викидати у каналізацію чи домашні контейнери для відходів. Необхідно запитати у фармацевта, як видалити лікарські засоби, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище.
6. Зміст упаковки та інші відомості
Що містить препарат Гемосол Б0
Активні речовини перед змішуванням та після змішування наведені нижче.
Активні речовини перед змішуванням:
1000 мл розчину, що міститься у малій камері (А), містить:
Хлорид кальцію, 2Н О
5,145 г
Хлорид магнію, 6Н О
2,033 г
Молочна кислота
5,4 г
1000 мл розчину, що міститься у великій камері (Б), містить:
Бікарбонат натрію
3,09 г
Хлорид натрію
6,45 г
Активні речовини після змішування:
Склад розчину (5000 мл) після змішування вмісту камери А (250 мл) та камери Б (4750 мл) такий:
ммоль/л
Кальцій, Ca
1,75
Магній, Mg
0,5
Натрій, Na
140
Хлориди, Cl
109,5
Молочні кислоти
3
Бікарбонати, HCO
32
Теоретична осмоларність: 287 мОсм/л
Інші складові частини:діоксид вуглецю (Е 290) та вода для ін'єкцій.
Як виглядає препарат Гемосол Б0 та що містить упаковка
Препарат Гемосол Б0 міститься у двокамерному мішку. Мішок розміщений у прозорому зовнішньому пакуванні.
Для отримання готового до застосування розчину необхідно зламати ламану затичку та змішати обидва розчини.
Готовий до застосування розчин є прозорим та безбарвним. Кожен мішок (А+Б) містить 5000 мл розчину для гемофільтрації, гемодіафільтрації та (або) гемодіалізу.
Кожна коробка містить два мішки та одну вкладиш для пацієнта.
Відповідальний суб'єкт
Vantive Belgium SRL
Бульвар д'Англетер, 2
1420 Брен-л'Аллєд
Бельгія
Виробник
Bieffe Medital S.p.A.,
вул. Стельвіо, 94,
23035 Сондальо (СО),
Італія
або
Vantive Manufacturing Limited,
вул. Мунін,
Каслбар,
графство Мейо
F23 XR63
Ірландія
Цей препарат дозволений до обігу в країнах-членах Європейського економічного простору та у Великій Британії (Північній Ірландії) під наступними назвами:
Австрія, Бельгія, Болгарія, Хорватія, Кіпр, Чехія, Данія, Естонія, Фінляндія, Франція, Німеччина,
Греція, Ісландія, Ірландія, Латвія, Литва, Люксембург, Мальта, Нідерланди, Норвегія, Польща, Португалія,
Словаччина, Словенія, Іспанія, Швеція, Велика Британія (Північна Ірландія): Гемосол Б0.
Дата останньої актуалізації вкладишу: вересень 2024 р. -------------------------------------------------------------------------------------------------------------------------
Інформація, призначена лише для фахівців охорони здоров'я
Гемосол Б0 розчин для гемодіалізу/гемофільтрації
Заходи обережності
Необхідно суворо дотримуватися інструкції щодо застосування препарату Гемосол Б0.
Розчини з обох камер мусятьбути змішані перед застосуванням.
Застосування забрудненого розчину для гемофільтрації може спричинити сепсис, шок та смерть пацієнта.
Для підвищення комфорту пацієнта препарат Гемосол Б0 можна підігріти до температури 37°C. Підігрівання розчину перед застосуванням необхідно здійснити перед відновленням та виключно з використанням сухого джерела тепла. Розчинів не слід підігрівати у водяній ванні чи мікрохвильовій печі. Оскільки розчин та упаковка на це дозволяють, перед введенням необхідно візуально перевірити розчин для виявлення наявності твердих частинок та зміни забарвлення. Не вводити, якщо розчин не є прозорим або спав є пошкодженим.
Додаткова заміна бікарбонату натрію може збільшити ризик розвитку метаболічної алкалози.
Перед початком лікування та під час його тривалості необхідно суворо контролювати електролітну та кислотно-лужну рівновагу. Оскільки Гемосол Б0 не містить калію, концентрація калію у сироватці крові повинна бути контролювана перед та під час гемофільтрації та (або) гемодіалізу.
Може знадобитися доповнення калію.
До розчину можна додати фосфати у кількості до 1,2 ммоль/л. У разі додавання фосфату калію загальна концентрація калію не повинна перевищувати 4 мЕкв/л (4 ммоль/л).
Об'єм та швидкість, з якою застосовується препарат Гемосол Б0, залежать від концентрації електролітів у крові, кислотно-лужної рівноваги та загального клінічного стану пацієнта.
Спосіб введення (дозу, швидкість інфузії та загальний об'єм) препарату Гемосол Б0 повинен бути встановлений лікарем. Континуюча гемофільтрація видаляє надмірну рідину та електроліти.
Якщо виникне порушення рівноваги рідин, необхідно суворо контролювати клінічний стан пацієнта та у разі потреби виправити рівновагу рідин.
Якщо пацієнт страждає на ниркову недостатність, унаслідок передозування може виникнути перегідратування та можуть виникнути серйозні наслідки, такі як застійна ниркова недостатність, порушення електролітної чи кислотно-лужної рівноваги.
Оскільки розчин не містить глюкози, його введення може привести до виникнення гіпоглікемії.
Необхідно регулярно контролювати концентрацію глюкози у крові.
Гемосол Б0 містить бікарбонат (двувуглець) та молочну кислоту (попередник бікарбонату), які можуть впливати на кислотно-лужну рівновагу пацієнта. Якщо під час лікування препаратом Гемосол Б0 виникне або погіршиться метаболічна алкалоз, може знадобитися зменшення швидкості введення або зупинка введення препарату.
Дозування
Загально прийнята швидкість потоку заміщувального розчину при гемофільтрації та гемодіафільтрації становить:
Дорослі:
500-3000 мл/год.
Загально прийнята швидкість потоку діалізного розчину (діалізату) при континуючому гемодіалізі становить:
Дорослі:
500-2500 мл/год.
У дорослих зазвичай застосовується загальна швидкість потоку, яка становить від близько 2000 до 2500 мл/год, що відповідає добовому об'єму рідини, який перебуває у межах від близько 48 до 60 л.
Діти та підлітки
Діапазон швидкості потоку заміщувального розчину при гемофільтрації та гемодіафільтрації та діалізного розчину (діалізату) при континуючому гемодіалізі становить:
Діти (від новонароджених до підлітків до 18 років): 1000-2000 мл/год/1,73 м .
Потрібна швидкість потоку може становити до 4000 мл/год/1,73 м , особливо у молодших дітей (≤10 кг). Абсолютна швидкість потоку (у мл/год) у дітей та підлітків зазвичай не повинна перевищувати максимальну швидкість потоку, застосовувану у дорослих.
Інструкція щодо застосування
Для отримання готового до застосування розчину розчин електролітів (мала камера А) необхідно додати до розчину буферної речовини (велика камера Б) після злому ламаної затички безпосередньо перед застосуванням.
Застосовувати виключно з відповідним обладнанням для позаустrojового лікування ниркової недостатності.
Під час процедури та введення препарату пацієнту необхідно застосовувати асептичну техніку.
Використовувати виключно тоді, коли зовнішня захисна упаковка не пошкоджена, всі шви цілі, ламана затичка не пошкоджена, а розчин прозорий. Міцно стиснути мішок, щоб перевірити його цілісність. У разі виявлення витоку розчин необхідно негайно видалити, оскільки не можна гарантувати стерильність.
Велика камера Б оснащена портом для ін'єкцій, який дозволяє після відновлення розчину додати інші необхідні лікарські засоби. Лікар відповідає за оцінку сумісності додаткового лікарського засобу з препаратом Гемосол Б0 шляхом перевірки, чи не виникають зміни кольору та (або) осадження, виникнення неріворозчинних комплексів або кристалів. Перед додаванням лікарського засобу необхідно перевірити, чи він розчиняється та стабільний у воді з pH, рівним pH препарату Гемосол Б0 (pH готового до застосування розчину становить 7,0-8,5). Додаткові складові частини можуть бути не сумісними з розчином. Необхідно ознайомитися з інструкцією щодо застосування додаваного лікарського засобу.
Необхідно видалити рідину з порту для ін'єкцій, утримувати мішок дном догори, введення лікарського засобу до порту для ін'єкцій та повністю перемішати. Необхідно негайно розпочати введення розчину.
Введення та перемішування додаткових складових частин завжди повинні здійснюватися перед підключенням мішка з розчином до позаустrojового обводу.
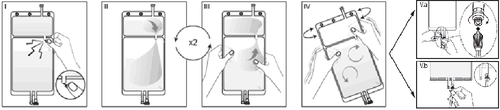
I
Безпосередньо перед застосуванням зняти зовнішню упаковку з мішка та видалити всі решти матеріали упаковки. Відкрити захисний покрив, зламавши ламану затичку, яка розташована між двома камерами мішка. Ламана затичка залишається у мішку.
(Див. рисунок I нижче).
II
Переконатися, що весь рідина з малої камери А був перекачаний до великої камери Б. (Див. рисунок II нижче).
III
Прополоскати двічімалу камеру А, виштовхуючи змішаний розчин назад до малої камери А, а потім знову до великої камери Б. (Див. рисунок III нижче).
IV
Якщо мала камера А порожня: потрясти велику камеру Б для повного перемішування її вмісту. Тепер розчин готовий до застосування, і мішок можна підвісити на стійку. (Див. рисунок IV нижче).
V
До кожного з двох портів доступу можна підключити лінію діалізу або обміну.
V.a
Якщо використовується доступ типу луер, видалити затичку, повернувши її та потягнувши, а потім підключити чоловічий кінець типу луер лок лінії діалізу або обміну до жіночого кінця типу луер рецептора на мішку, натиснувши на нього та повернувши. Переконатися, що з'єднання є повністю осаджене та певне. Тепер з'єднання відкрито. Перевірити, чи тече рідина вільно.
(Див. рисунок V.a нижче).
Коли лінії діалізу або обміну від'єднані від з'єднання типу луер, з'єднання закривається та припиняється потік рідини. Порт типу луер безігловий та можна протирати дезинфікуючими засобами.
V.bЯкщо використовується порт для ін'єкцій, спочатку видалити затичку шляхом її злому. Порт для ін'єкцій можна протирати дезинфікуючими засобами. Потім проколити гумову перегородку голкою. Перевірити, чи тече рідина вільно. (Див. рисунок V.b нижче).
Готовий до застосування розчин необхідно застосувати негайно після видалення зовнішньої упаковки.
Якщо готовий до застосування розчин не буде негайно застосований, його необхідно застосувати протягом 24 годин, включаючи час лікування, після додавання розчину електролітів до розчину буферної речовини.
Готовий до застосування розчин призначений виключно для одноразового застосування. Необхідно видалити невикористаний розчин негайно після застосування.
Всі невикористані залишки лікарського засобу або його відходи необхідно видалити згідно з місцевими правилами.
- Країна реєстрації
- Потрібен рецептНі
- ІмпортерBieffe Medital S.p.A. Vantive Manufacturing Limited
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
Лікарі онлайн щодо Гемосол Бо
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Гемосол Бо – за рішенням лікаря та згідно з місцевими правилами.














