HEXVIX 85 mg PÓ E SOLVENTE PARA SOLUÇÃO INTRAVESICAL

Pergunte a um médico sobre a prescrição de HEXVIX 85 mg PÓ E SOLVENTE PARA SOLUÇÃO INTRAVESICAL

Como usar HEXVIX 85 mg PÓ E SOLVENTE PARA SOLUÇÃO INTRAVESICAL
Introdução
Prospecto: informação para o paciente
HEXVIX 85 mg pó e dissolvente para solução intravesical
Hexaminolevulinato
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto. Pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou enfermeiro.
- Se experimentar efeitos adversos, consulte o seu médico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto:
- O que é Hexvix e para que é utilizado
- O que precisa saber antes de que lhe administrem Hexvix
- Como usar Hexvix
- Possíveis efeitos adversos
- Conservação de Hexvix
- Conteúdo do envase e informação adicional.
1. O que é hexvix e para que é utilizado
Este medicamento é exclusivamente para uso diagnóstico.
Este medicamento é utilizado para ajudar na detecção do cancro da bexiga. É administrado antes de o seu médico utilizar um dispositivo especial chamado “cistoscópio” que lhe permite visualizar o interior da sua bexiga. Um cistoscópio ajuda a visualizar possíveis tumores e, portanto, a eliminar as células anormais, que se iluminam em luz azul, após a administração de Hexvix.
2. O que precisa saber antes de que lhe administrem HEXVIX
Não use Hexvix:
- Se é alérgico (hipersensível) ao princípio ativo ou a qualquer um dos outros componentes de Hexvix, incluído o líquido utilizado para dissolver (ver Seção 6 Informação adicional).
- Se padece uma porfiria (uma doença sanguínea rara e hereditária)
Advertências e precauções:
Consulte o seu médico ou enfermeiro antes de começar a usar Hexvix.
- Se padece uma infecção urinária ou se sente ardor/escozor ao urinar.
- Se se submeteu recentemente a uma terapia com BCG na bexiga.
- Se lhe foi realizada recentemente uma operação de bexiga.
Estas circunstâncias podem causar reações locais na sua bexiga, o que pode dificultar ao seu médico a interpretação do que observar durante o exame.
Outros medicamentos e Hexvix:
Comunique ao seu médico se está a tomar ou tomou recentemente outros medicamentos, mesmo aqueles adquiridos sem receita.
Fertilidade, gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico antes de utilizar este medicamento.
Condução e uso de máquinas
Consulte o seu médico sobre a condução e o uso de máquinas após a administração de Hexvix.
3. Como usar Hexvix
Hexvix deve ser preparado e administrado por pessoal qualificado. Hexvix é geralmente administrado num hospital ou clínica.
O seu médico o administrará da seguinte forma:
- Um pequeno tubo denominado catéter será introduzido na sua bexiga.
- A sua bexiga será esvaziada através deste tubo.
- Hexvix será introduzido dentro da bexiga através deste tubo.
- Hexvix será mantido no interior da sua bexiga durante 60 minutos.
- Uma vez decorrido este tempo, a bexiga será esvaziada com o catéter.
- O seu médico utilizará um dispositivo denominado cistoscópio para a exploração da sua bexiga.
Se Vd. usa mais Hexvix do que deve
Não se espera que tenham lugar efeitos adversos em caso de aumento do tempo de permanência de Hexvix na bexiga por cima de 60 minutos ou do aumento da quantidade de Hexvix utilizada. Se está preocupado com respeito a este tema, consulte com o seu médico ou enfermeira.
4. Possíveis efeitos adversos
Assim como todos os medicamentos, Hexvix pode produzir efeitos adversos, embora não todas as pessoas os sofram. Existe risco de possíveis efeitos adversos relativos à técnica (cistoscopia) utilizada para explorar a sua bexiga. Geralmente, a utilização de Hexvix como método complementar à cistoscopia estándar para um diagnóstico mais preciso do cancro da bexiga é bem tolerado. Se ocorrem efeitos adversos, serão os típicos associados à técnica de exame, normalmente não são graves nem prolongados no tempo. Podem aparecer os seguintes efeitos adversos após o processo de exploração utilizando este medicamento:
Frequentes(podem afetar até 1 de cada 10 pessoas):
- Sensação de ganas de vomitar (náuseas), vómitos.
- Diarreia.
- Prisão de ventre.
- Calambre muscular ou dor no e ao redor do estômago (abdomen).
- Dor ou dificuldade ao urinar.
- Incapacidade para esvaziar a bexiga (retenção urinária).
- Sangue na urina.
- Dor após a exploração (procedimento).
- Febre (temperatura elevada)
Pouco frequentes(podem afetar até 1 de cada 100 pessoas):
- Dor de cabeça
- Sensação de queimadura ao passar a urina (causado por infecção ou inflamação na bexiga).
- Necessidade frequente de urinar.
- Envenenamento da sangue (septicemia).
- Incapacidade para dormir ou dificuldade para conciliar o sono.
- Dor no tubo chamado uretra, através do qual passa a urina.
- Sensação contínua de ganas de urinar (e com urgência).
- Aumento dos recuentos de glóbulos brancos, aumento das concentrações de bilirrubina (um pigmento amarelo da bile) ou das enzimas hepáticas, tudo isso deveria ser observado nos resultados dos análises de sangue.
- Diminuição do número de glóbulos vermelhos do organismo (anemia).
- Inflamação do glande do pênis (balanite).
- Dor de costas.
- Gota.
- Exantema (sarpullido, erupção da pele).
- Coceira (prurido).
Frequência não conhecida(não pode ser estimada a partir dos dados disponíveis):
- Choque anafilactoide (queda da pressão sanguínea, aumento do ritmo cardíaco, erupção na pele)
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano. www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Hexvix
Mantenha este medicamento fora da vista e do alcance das crianças.
Não use este medicamento uma vez ultrapassada a data de validade que figura no embalagem exterior. A data de validade refere-se ao último dia do mês.
Pó e dissolvente: o produto não requer condições especiais de conservação.
Solução (após realizar a mistura): conservar entre 2 ºC e 8 ºC (na geladeira) durante um período de tempo máximo de 2 horas.
O pessoal do hospital deve assegurar-se de que o produto é conservado e eliminado de forma adequada e de que não é utilizado com posterioridade à data de validade impressa no embalagem exterior.
6. Conteúdo do envase e informação adicional
Composição de Hexvix
?O princípio ativo é hexaminolevulinato em forma de cloreto.
?O resto dos ingredientes são fosfato de dissódio, dihidrogenofosfato de potássio, cloreto de sódio, ácido clorídrico, hidróxido de sódio e água para preparações injetáveis
Aspecto do produto e conteúdo do envase
- Cada envase contém um frasco de pó, de cor branca a cor de osso ou amarelo pálido, que contém 85 mg do princípio ativo hexaminolevulinato (como cloreto), e uma seringa pré-carregada, que contém 50 ml de um líquido transparente e incolor para dissolver o pó.
- O pó de Hexvix é dissolvido em 50 ml da solução fornecida no envase. Uma vez misturado o pó com o dissolvente, obtém-se uma solução que contém 1,7 mg/ml de hexaminolevulinato, o que corresponde a 8 mmol/l de solução de hexaminolevulinato.
Título da autorização de comercialização e responsável pela fabricação:
Photocure ASA
Hoffsveien ,4
NO-0275 Oslo,
Noruega
Pode solicitar mais informações sobre este medicamento dirigindo-se ao título da autorização de comercialização.
Este medicamento foi autorizado com o nome comercial Hexvix nos seguintes estados membros do Espaço Económico Europeu e no Reino Unido (Irlanda do Norte):Áustria, Bélgica, República Checa, Dinamarca, Estónia, Finlândia, França, Alemanha, Grécia, Hungria, Irlanda, Islândia, Itália, Letónia, Lituânia, Países Baixos, Noruega, Polónia, Portugal, Eslovénia, Espanha, Suécia e Reino Unido (Irlanda do Norte).
Data da última revisão deste prospecto:Janeiro 2022
A informação detalhada e atualizada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es
Esta informação está destinada unicamente a médicos ou profissionais do setor sanitário:
Instruções de manipulação
O hexaminolevulinato pode causar sensibilização através do contacto com a pele.
Todos os passos devem ser realizados com material estéril e em condições de assepsia.
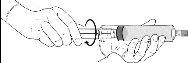
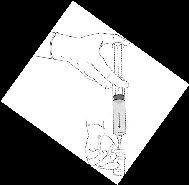
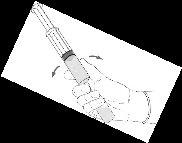
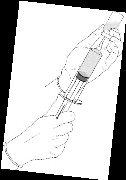
Procedimento de reconstituição: pó de Hexvix e dissolvente para Hexvix em seringa pré-carregada
|
|
|
|
|
|
|
|
|
|
Hexvix está agora reconstituído e pronto para usar. O aspecto da solução reconstituída é uma solução clara ou ligeiramente opalescente, e entre incolor e amarelo pálido.
Adicionar duas horas à hora atual e escrever o tempo de validade resultante e a data na etiqueta da seringa
Este produto é para um único uso. Deve ser descartado todo o resto de produto sobrante. Não há requisito especial para a sua eliminação.
Foi demonstrado que a solução conserva a sua estabilidade química e física durante um período de 2 horas a 2 ºC – 8 ºC. Do ponto de vista microbiológico, o produto deve ser utilizado de forma imediata. De não ser assim, os tempos e condições de conservação antes do seu uso são responsabilidade do usuário e normalmente não devem exceder as 2 horas a 2 ºC - 8 ºC.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a HEXVIX 85 mg PÓ E SOLVENTE PARA SOLUÇÃO INTRAVESICALForma farmacêutica: INJETÁVEL, 25 mg brometo de edrofônio/2 mlSubstância ativa: edrophoniumFabricante: Mana Pharma S.L.Requer receita médicaFabricante: Sociedad Española De Carburos Metalicos S.A.Requer receita médicaFabricante: Sociedad Española De Carburos Metalicos S.A.Requer receita médica
Médicos online para HEXVIX 85 mg PÓ E SOLVENTE PARA SOLUÇÃO INTRAVESICAL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de HEXVIX 85 mg PÓ E SOLVENTE PARA SOLUÇÃO INTRAVESICAL – sujeita a avaliação médica e regras locais.