
EDUNIX 2,6 mg/ml SOLUÇÃO ORAL
Pergunte a um médico sobre a prescrição de EDUNIX 2,6 mg/ml SOLUÇÃO ORAL

Como usar EDUNIX 2,6 mg/ml SOLUÇÃO ORAL
Introdução
Prospecto: informação para o paciente
Edunix 2,6 mg/ml solução oral
Hidrocloruro de hidromorfona
Para uso em adolescentes a partir de 12 anos e adultos
Leia todo o prospecto detenidamente antes de começar a tomar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, embora tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Edunix e para que se utiliza
- O que precisa saber antes de começar a tomar Edunix
- Como tomar Edunix
- Posíveis efeitos adversos
- Conservação de Edunix
- Conteúdo do envase e informações adicionais
1. O que é Edunix e para que se utiliza
A solução oral foi prescrita para aliviar a dor intensa.
Contém o princípio ativo hidromorfona, que é um analgésico forte ('calmante') que pertence ao grupo de medicamentos chamados analgésicos opiáceos.
2. O que precisa saber antes de começar a tomar Edunix
Não tome Edunix
- se é alérgico ao hidrocloruro de hidromorfona ou a algum dos outros componentes deste medicamento (incluídos na seção 6, Informações adicionais);
- se tem problemas respiratórios, como doença obstructiva crônica grave das vias respiratórias, depressão respiratória ou asma grave. Os sintomas podem incluir dispnéia, tosse ou respiração mais lenta e débil do que o esperado;
- se tem problemas de estômago ou dor abdominal inesperada (abdomen agudo);
- se tem um problema intestinal com ausência de motilidade (íleo paralítico);
- se está tomando inibidores da monoamino oxidase (por exemplo, tranilcipromina, fenelzina, isocarboxazida, moclobemida e linezolida), ou se tomou este tipo de medicamento nas últimas 2 semanas.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a tomar hidrocloruro de hidromorfona se lhe for aplicável alguma das seguintes situações:
- problemas para respirar com normalidade (como a doença pulmonar obstructiva crônica ou capacidade respiratória reduzida como a asma); os sintomas podem incluir dispnéia e tosse; ter dificuldades para dormir (apneia do sono);
- tem um forte dor de cabeça ou se sente mal devido a um aumento da pressão cerebral ou lesão na cabeça (por exemplo, devido a uma doença cerebral). Isso se deve a que a solução oral pode piorar os sintomas ou ocultar a extensão de uma lesão na cabeça;
- sofre ataques, convulsões ou crises epilépticas;
- padece um transtorno mental como consequência de uma intoxicação (psicose tóxica);
- tem a tensão arterial baixa (hipotensão);
- se sente fraco ou mareado;
- tem problemas biliares, ataque biliar ou de rim;
- tem dor ou molestias abdominais de tipo cólico;
- tem inflamação do pâncreas (que pode causar dor intensa no abdômen e nas costas);
- padece uma obstrução intestinal ou transtornos inflamatórios intestinais;
- tem um aumento da próstata, o que provoca dificuldade para urinar (em homens);
- tem a função reduzida da glândula suprarrenal, por exemplo, doença de Addison (a glândula suprarrenal não funciona corretamente);
- tem baixa atividade da tireoide (hipotireoidismo);
- tem problemas renais ou hepáticos graves;
- se si ou algum membro da sua família tem antecedentes de abuso ou dependência do álcool, de medicamentos de venda com receita ou de substâncias ilícitas (“adicção”);
- se fuma;
- se já teve problemas com o seu estado de ânimo (depressão, ansiedade ou um transtorno de personalidade) ou recebeu tratamento de um psiquiatra para outras doenças mentais;
- tem sintomas de abstinência como agitação, ansiedade, tremores ou suoração ao deixar de tomar álcool ou drogas;
- pacientes de idade avançada ou debilitados;
- padece constipação.
Transtornos respiratórios relacionados com o sono
Hidromorfona pode causar transtornos respiratórios relacionados com o sono como apneia do sono (pausa da respiração durante o sono) e hipoxemia relacionada com o sono (níveis baixos de oxigênio no sangue). Os sintomas podem incluir interrupções da respiração durante o sono, despertares noturnos devido à dificuldade para respirar, dificuldade para manter o sono ou sonolência excessiva durante o dia. Se si ou outra pessoa observa estes sintomas, consulte o seu médico. O seu médico pode considerar diminuir a dose.
Pode experimentar mudanças hormonais enquanto toma esta solução oral. Pode que o seu médico queira controlar estas mudanças.
Pode experimentar uma maior sensibilidade à dor apesar de estar tomando doses altas da solução oral (hiperalgesia). O seu médico decidirá se precisa de uma mudança de dose ou de um cambio de analgésico forte ('calmante').
Se vai ser submetido a uma operação, informe o médico de que está tomando esta solução oral.
O conteúdo da solução oral não deve ser injetado nunca, porque pode provocar efeitos adversos graves que podem ser mortais.
Este medicamento contém hidromorfona, que é um opioide. O uso repetido de analgésicos opioides pode reduzir a eficácia do fármaco (o seu organismo se acostuma com o fármaco).
O uso repetido de hidromorfona pode causar dependência e abuso, o que pode provocar uma sobredose potencialmente mortal. É importante que informe o seu médico se pensa que pode ter desenvolvido dependência deste medicamento.
Outros medicamentos e Edunix
Informe o seu médico ou farmacêutico se está tomando, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Se tomar esta solução oral com algum outro medicamento, o efeito da solução oral ou do outro medicamento pode ser modificado.
Esta solução oral não deve ser utilizada junto com um inibidor da monoamino oxidase, ou se tomou este tipo de medicamento nas últimas duas semanas (ver seção 2 'Não tome Edunix').
Informe o seu médico ou farmacêutico se está tomando:
- medicamentos que o ajudem a dormir ou a manter a calma (por exemplo, tranquilizantes, hipnóticos ou sedantes, incluídas as benzodiazepinas);
- medicamentos conhecidos como barbitúricos para tratar ataques ou para ajudá-lo a dormir;
- medicamentos para deixar de se sentir ou estar doente;
- medicamentos para prevenir ou aliviar os sintomas de alergia (antihistamínicos);
- medicamentos para tratar a depressão;
- medicamentos para tratar transtornos psiquiátricos ou mentais (antipsicóticos como as fenotiazinas);
- outros analgésicos fortes (“calmantes”).
Informe também o seu médico se lhe foi administrado recentemente um anestésico.
O uso concomitante de hidromorfona e benzodiazepinas (que podem ajudar a reduzir a ansiedade e as crises, relaxar os músculos e induzir o sono) aumenta o risco de sonolência, dificuldades para respirar (depressão respiratória) e coma, e pode ser potencialmente mortal. Por isso, só se deve considerar o uso concomitante quando não forem possíveis outras opções de tratamento. O uso concomitante de opioides e fármacos utilizados para tratar a epilepsia, a dor de nervo ou a ansiedade (gabapentina e pregabalina) aumenta o risco de sobredose por opioides e depressão respiratória, e pode ser potencialmente mortal.
No entanto, se o seu médico lhe prescreve Edunix junto com medicamentos sedantes, o seu médico deve limitar a dose e a duração do tratamento concomitante.
Informe o seu médico de todos os medicamentos sedantes que está tomando e siga atentamente a dose recomendada pelo seu médico. Pode ser útil informar amigos ou familiares que estejam a par dos sinais e sintomas indicados anteriormente. Entre em contato com o seu médico quando experimentar ditos sintomas.
Toma de Edunix com comidas, bebidas ou álcool
Esta solução oral pode ser tomada com ou sem alimentos, mas se recomenda não beber álcool enquanto estiver tomando Edunix.
Beber álcool durante o tratamento com esta solução oral pode produzir sonolência ou afetar negativamente a sua respiração.
Gravidez e lactação
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Gravidez
Não se recomenda o uso de Edunix durante a gravidez e o parto a menos que seja especificamente indicado pelo seu médico. Dependendo da dose e da duração do tratamento com hidromorfona, pode produzir-se uma respiração lenta e superficial (depressão respiratória) ou sintomas de abstinência no recém-nascido. Os recém-nascidos podem sofrer efeitos de abstinência (como choro agudo, nervosismo, ataques, falta de apetite e diarreia) se as suas mães tomaram hidromorfona de forma prolongada durante a gravidez.
Lactação
Hidromorfona pode passar para o leite materno. Por isso, Edunix não deve ser utilizado se está em período de lactação.
Condução e uso de máquinas
Esta solução oral pode produzir uma série de efeitos adversos como sonolência que pode afetar a sua capacidade para conduzir ou utilizar máquinas (ver seção 4 “lista completa de efeitos adversos”). Estes efeitos são mais evidentes ao começar a tomar a solução oral ou ao aumentar a dose. Se se sentir afetado, não deve conduzir nem utilizar máquinas.
Edunix contém parahidroxibenzoato de metilo
Pode produzir reações alérgicas (possivelmente retardadas) porque contém parahidroxibenzoato de metilo.
Edunix contém sacarose
Este medicamento contém sacarose. Se o seu médico lhe indicou que padece uma intolerância a certos açúcares, consulte com ele antes de tomar este medicamento.
Pode produzir cáries.
Edunix contém sódio
Este medicamento contém menos de 23 mg de sódio (1mmol) por comprimido de liberação prolongada; isto é, essencialmente “exento de sódio”.
3. Como tomar Edunix
Tome sempre a solução oral exatamente como lhe indicou o seu médico. A etiqueta do seu medicamento lhe indicará que quantidade de solução oral deve tomar e com que frequência.
Não exceda a dose recomendada pelo seu médico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
Adultos e adolescentes maiores de 12 anos
A dose inicial habitual é de 0,5 ml (1,3 mg) ou 1,0 ml (2,6 mg) de solução oral cada 4 horas. No entanto, o seu médico lhe prescreverá a dose necessária para aliviar a sua dor. Se notar que continua sentindo dor enquanto toma esta solução oral, comente com o seu médico.
Crianças menores de 12 anos
Não se recomenda o uso deste medicamento em crianças menores de 12 anos.
Pacientes de idade avançada e pacientes com problemas renais ou hepáticos
Informe o seu médico se padece problemas renais ou hepáticos. O seu médico pode prescrever uma dose mais baixa desta solução oral se for um paciente de idade avançada ou tiver problemas de rim ou fígado.
Modo de administração
Este medicamento é para uso oral.
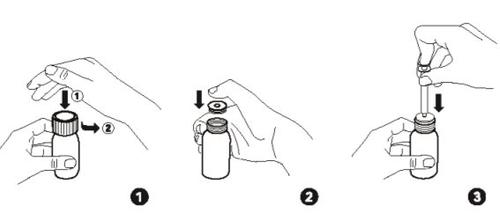
- Abra o frasco: Pressione o tampão de rosca à prova de crianças e gire-o no sentido contrário ao dos ponteiros do relógio (Fig. 1). Nota: Tenha à mão o tampão de rosca para poder voltar a fechar o frasco com o tampão imediatamente após cada uso.
- Apenas para o primeiro uso:Coloque o frasco sobre uma superfície plana. Introduza firmemente com o polegar o adaptador de plástico no gargalo da garrafa, se for fornecido separadamente (fig. 2). Se o adaptador já estiver fixado na garrafa, omita o passo da Fig. 2.
- Pegue a seringa e verifique se o êmbolo da seringa está completamente pressionado.
- Mantenha o frasco na posição vertical e introduza firmemente a seringa aplicadora no adaptador de plástico (Fig. 3).
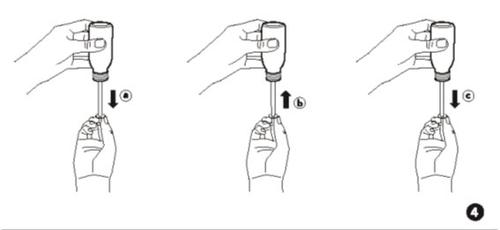
- Dê a volta ao frasco e à seringa.
- Puxe lentamente o êmbolo para baixo até o topo, para que a seringa se encha com o medicamento (Fig. 4a). Em seguida, empurre o êmbolo completamente para cima, para eliminar as bolhas de ar que possam estar no interior da seringa de aplicação (Fig. 4b).
- Em seguida, retire o êmbolo lentamente, até a quantidade (marca) que precisa para a sua dose (Fig. 4c).
- Vire novamente toda a garrafa com a seringa para cima. Com o polegar da mão segurando a garrafa, coloque o adaptador e retire a seringa da garrafa (Fig. 5).
- Agora, pode tomar a dose do medicamento diretamente da seringa. Para isso, lembre-se de sentar-se ereto e pressionar o êmbolo da seringa lentamente para poder engolir a dose corretamente. Também pode misturar a dose do medicamento em uma bebida sem álcool. Se fizer isso, deve tomar essa bebida imediatamente após misturá-la.
- Voltar a fechar o frasco após o uso com o tampão de rosca à prova de crianças. Nota: O adaptador permanece na garrafa (Fig. 6).
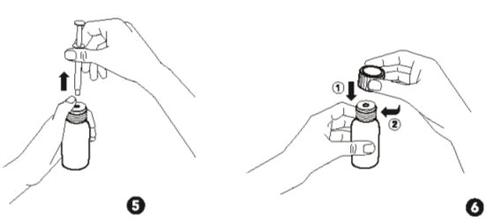
- Limpeza:Após o uso, limpe o exterior da seringa com um pano limpo e seco.
Se tomar mais Edunix do que deve ou se alguém tomar acidentalmente a sua solução oral
Se tomou mais solução oral do que deve, ligue imediatamente ao seu médico ou ao hospital. Em caso de sobredose ou ingestão acidental, consulte o seu médico ou ligue ao Serviço de Informação Toxicológica; Telefone 91 562 04 20, indicando o medicamento e a quantidade tomada.
As pessoas que tomaram uma sobredose podem se sentir muito sonolentas, doentes ou mareadas e também podem desenvolver pupilas contraídas, problemas respiratórios, pressão arterial baixa ou pneumonia causada pela inalação de vômito ou corpos estranhos (os sintomas podem incluir dispnéia, tosse e febre). Em casos graves de colapso circulatório ou inconsciência profunda (coma) pode ocasionar a morte. Quando for ao médico, certifique-se de levar consigo este prospecto e qualquer resto de solução oral para mostrá-los ao médico.
Se tomou demasiada solução oral, em nenhum caso deve expor-se a situações que requeiram uma concentração elevada, por exemplo, conduzir um carro.
Se esqueceu de tomar Edunix
Se esqueceu de tomar uma dose, tome-a assim que se lembrar e continue como antes. Não tome duas doses em um período de 4 horas. Não tome uma dose dupla para compensar a dose esquecida.
Se interromper o tratamento com Edunix
Não deixe de tomar repentinamente esta solução oral a menos que o seu médico o indique. Se deseja deixar de tomar a sua solução oral, comente primeiro com o seu médico. Ele lhe indicará como fazer isso, normalmente reduzindo gradualmente a dose para que não experimente efeitos adversos. Pode aparecerem sintomas de abstinência como agitação, ansiedade, nervosismo, dificuldade para dormir, hiperatividade incomum, tremores ou transtornos gastrointestinais (por exemplo, mal-estar estomacal) se deixar de tomar repentinamente esta solução oral.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Efeitos adversos possíveis
Tal como todos os medicamentos, este medicamento pode provocar efeitos adversos, embora nem todas as pessoas os sofram.
Este medicamento pode causar reações alérgicas (hipersensibilidade) que podem ser graves (reações anafiláticas). A frequência destas reações é desconhecida. Informe o seu médico imediatamente se tiver dificuldade em respirar, inchaço de pálpebras, face, lábios, boca ou garganta ou qualquer erupção cutânea ou picazón, especialmente aquelas que cobrem todo o corpo.
A respiração lenta e débil (depressão respiratória) é o efeito adverso mais grave da sobredose por opioides.
Como ocorre com todos os analgésicos potentes, existe o risco de se tornar viciado ou dependente desta solução oral.
Muito frequentes(podem afetar mais de 1 em cada 10 pessoas):
- Prisão de ventre (o seu médico pode prescrever-lhe um laxante para este problema).
- Sensação de mal-estar.
- Tonturas, sonolência.
Frequentes(podem afetar até 1 em cada 10 pessoas):
- Mal-estar (normalmente desaparece após alguns dias, mas o seu médico pode prescrever-lhe um medicamento se o problema persistir).
- Ansiedade, confusão.
- Dificuldade em dormir.
- Secura na boca, perda de apetite, dor abdominal ou desconforto abdominal.
- Dor de cabeça.
- Sensação de fraqueza.
- Picazón na pele.
- Sudorese.
- Necessidade repentina de urinar.
Pouco frequentes(podem afetar até 1 em cada 100 pessoas):
- Sintomas de abstinência (ver seção 3 «Se interromper o tratamento com Edunix»).
- Dispepsia, diarreia, distúrbios do paladar.
- Depressão, sensação de felicidade extrema (euforia), alucinações, pesadelos.
- Visão turva.
- Agitação.
- Temor, espasmos musculares, formigamento ou entorpecimento.
- Pressão arterial baixa.
- Dificuldade em respirar.
- Diminuição do desejo sexual, impotência.
- Erupção cutânea, urticária.
- Inchaço de mãos, tornozelos ou pés (acumulação de líquido nos tecidos).
- Dificuldade em urinar.
- Mal-estar geral.
- Cansaço.
- Piora dos testes de função hepática (em uma análise de sangue).
Raros(podem afetar até 1 em cada 1.000 pessoas):
- Agresividade.
- Sentir-se mais sonolento do que o normal.
- Falta de energia.
- Ritmo cardíaco rápido, ritmo cardíaco lento, palpitações.
- Sibilâncias ou dificuldade em respirar.
- Mudanças na função pancreática (em uma análise de sangue).
Frequência desconhecida(não pode ser estimada a partir dos dados disponíveis):
- Apneia do sono (interrupções da respiração durante o sono).
- Ataques, crises ou convulsões.
- Mudanças de humor (disforia), inquietude.
- Aumento da sensibilidade à dor.
- Insuficiência intestinal (íleo paralítico).
- Constricção das pupilas.
- Sensação de calor.
- Movimentos musculares incontrolados.
- Erupção cutânea com picazón (urticária).
- Necessidade de tomar doses mais altas para obter o mesmo nível de alívio da dor (tolerância).
- Síndrome de abstinência de drogas em recém-nascidos cujas mães tomaram Edunix durante a gravidez (ver seção 2).
Se tiver algum efeito adverso, informe o seu médico ou farmacêutico. Isso inclui os efeitos adversos não mencionados neste prospecto.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema de notificação incluído no Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano. Website: www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Edunix
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no envase e na etiqueta, após CAD. A data de validade é o último dia do mês que se indica.
Conservar abaixo de 25°C. Manter no envase original.
Não use após 2 meses após a primeira abertura do frasco.
Os medicamentos não devem ser jogados nos deságues nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, você ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição de Edunix
- O princípio ativo é hidrocloruro de hidromorfona. Cada ml contém 2,6 mg de hidrocloruro de hidromorfona equivalente a 2,32 mg de hidromorfona.
- Os demais componentes são: parahidroxibenzoato de metilo (E-218), sacarose, glicerol 99% (E-422), ácido cítrico monohidrato (E-330), citrato de sódio (E-331) e água purificada.
Aspecto do produto e conteúdo do envase
Solução transparente, incolor, ligeiramente viscosa, de sabor e odor doce. Inclui uma seringa dosadora para a dosagem.
A solução oral é envasada em frascos de vidro marrom de 20, 50 ou 100 ml, fechados com tampa de rosca à prova de crianças com um anel à prova de manipulações. O frasco é introduzido em uma caixa plegável junto com uma seringa dosadora de plástico de 3 ml (graduação de 0,1 ml).
Pode ser que apenas alguns tamanhos de envase sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Aristo Pharma GmbH
Wallenroder Str. 8-10
13435 Berlim
Alemanha
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Aristo Pharma Iberia, S.L.
C/ Solana, 26
28850, Torrejón de Ardoz
Madri - Espanha
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu com os seguintes nomes:
Alemanha: Hydromorphon Aristo 2,6 mg/ml Lösung zum Einnehmen
Espanha: Edunix 2,6 mg/ml solução oral
Malta: Hydromorphone Aristo 2,6 mg/ml oral solution
Data da última revisão deste prospecto: janeiro 2025
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a EDUNIX 2,6 mg/ml SOLUÇÃO ORALForma farmacêutica: COMPRIMIDO DE LIBERTAÇÃO MODIFICADA, 16 mgSubstância ativa: hydromorphoneFabricante: Aristo Pharma GmbhRequer receita médicaForma farmacêutica: COMPRIMIDO DE LIBERTAÇÃO MODIFICADA, 32 mgSubstância ativa: hydromorphoneFabricante: Aristo Pharma GmbhRequer receita médicaForma farmacêutica: COMPRIMIDO DE LIBERTAÇÃO MODIFICADA, 4 mgSubstância ativa: hydromorphoneFabricante: Aristo Pharma GmbhRequer receita médica
Médicos online para EDUNIX 2,6 mg/ml SOLUÇÃO ORAL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de EDUNIX 2,6 mg/ml SOLUÇÃO ORAL – sujeita a avaliação médica e regras locais.














