
AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSE
Pergunte a um médico sobre a prescrição de AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSE

Como usar AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSE
Introdução
Prospecto: informação para o paciente
AKANTIOR 0,8 mg/ml colírio em solução em envase unidose
polihexanida
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é AKANTIOR e para que é utilizado
- O que precisa saber antes de começar a usar AKANTIOR
- Como usar AKANTIOR
- Possíveis efeitos adversos
- Conservação de AKANTIOR
- Conteúdo do envase e informação adicional
1. O que é AKANTIOR e para que é utilizado
AKANTIOR contém o princípio ativo polihexanida.
AKANTIOR é utilizado em adultos e crianças a partir de 12 anos de idade para tratar a queratite por Acanthamoeba. Acanthamoebaé um parasito (organismo diminuto que vive dentro dos seres humanos e que pode causar doença) que pode causar uma infecção que dá lugar a queratite (inflamação da córnea, a camada transparente da parte frontal do olho). A queratite por Acanthamoebapode causar defeitos graves na superfície da córnea, incluindo úlceras (feridas abertas).
AKANTIOR lesa a membrana (pele externa) do parasito Acanthamoebae causa a saída do conteúdo celular, o que destrói a célula. AKANTIOR também impede que o parasito Acanthamoebafaça cópias do seu DNA ao interferir com enzimas (proteínas) responsáveis pelo processo de replicação, o que interrompe o crescimento e a reprodução do parasito nos seres humanos.
2. O que é AKANTIOR e para que é utilizado
Não use AKANTIOR
Se é alérgico a polihexanida ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar AKANTIOR.
O tratamento com AKANTIOR pode causar molestias oculares de leves a moderadas (como dor ocular) e olho vermelho. Se experimentar uma reação ocular grave, entre em contato com o seu médico.
Crianças e adolescentes
Não se recomenda utilizar AKANTIOR em crianças menores de 12 anos, porque não foi estudado neste grupo de idade.
Outros medicamentos e AKANTIOR
Informa ao seu médico ou farmacêutico se está utilizando, utilizou recentemente ou possa ter que utilizar qualquer outro medicamento.
Se está utilizando outro colírio,espere pelo menos 5 minutos entre a aplicação de AKANTIOR e a aplicação do outro colírio. AKANTIOR deve ser administrado por último.
Gravidez e lactação
Não há experiência do uso de AKANTIOR em mulheres grávidas. Não se recomenda utilizar AKANTIOR durante a gravidez. Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Desconhece-se se AKANTIOR é excretado no leite materno. Consulte o seu médico ou farmacêutico antes de começar o tratamento com AKANTIOR.
Condução e uso de máquinas
A sua visão pode ser temporariamente borrosa após usar AKANTIOR. Não conduza nem use máquinas até que a sua visão seja clara novamente.
AKANTIOR contém fosfatos
Este medicamento contém 0,37 mg de fosfatos em cada gota equivalente a 10,66 mg/ml. Se sofre de dano grave na camada transparente da parte frontal do olho (córnea), o tratamento com fosfatos, em casos muito raros, pode provocar páiches nublados na córnea devido ao cálcio.
3. Como usar AKANTIOR
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico.
O tratamento consta de duas partes: tratamento intensivo durante os primeiros 19 dias e tratamento de continuação a partir do dia 20.
A dose recomendada é 1 gotade AKANTIOR no olho afetado tal como se indica a seguir:
Tratamento intensivo inicial (19 dias)
- Aplique uma gota a cada hora (16 vezes ao dia) durante os primeiros cinco dias (dias 1 a 5)
- Aplique uma gota a cada 2 horas (8 vezes ao dia) durante os seguintes sete dias (dias 6 a 12)
- Aplique uma gota a cada 3 horas (6 vezes ao dia) durante os seguintes sete dias (dias 13 a 19)
Tratamento de continuação
- Aplique uma gota a cada 4 horas (4 vezes ao dia) até que não haja inflamação corneal nem sinais de infecção (o olho está curado).
O seu médico indicará quando interromper o tratamento.
Instruções de uso
- Lave as mãos.
- Abra o sobrecartão de alumínio que contém os envases unidose.
- Separe o envase unidose da tira e coloque os envases sem abrir novamente no sobrecartão.
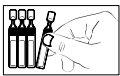
- Abra o envase unidose girando a parte superior sem puxá-la. Não toque a ponta após abrir o envase.
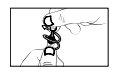
- Incline a cabeça para trás. O envase está agora aberto. Mantenha o envase unidose na posição vertical e não o pressione.
- Use um dedo para puxar suavemente para baixo a pálpebra inferior do olho afetado.
- Inverta o envase unidose e coloque a ponta do envase perto do seu olho. Não toque o olho nem a pálpebra com a ponta do envase.

- Pressione o envase unidose para administrar apenas uma gota e, em seguida, solte a pálpebra inferior.
- Feche o olho e pressione um dedo sobre o ângulo interno (nasal) do olho afetado. Mantenha a pressão por 2 minutos.
- Elimine o envase unidose após usá-lo.
Se usar mais AKANTIOR do que deve
Aplique a próxima dose na hora habitual, porque é improvável que cause danos graves.
Se esquecer de usar AKANTIOR
Aplique a próxima dose na hora habitual. Não use uma dose dupla para compensar as doses esquecidas.
Se interromper o tratamento com AKANTIOR
Use AKANTIOR tal como o médico indicou para conseguir o máximo efeito. Informe sempre o seu médico se planeia interromper o tratamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Assim como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
A maioria dos efeitos adversos costuma ocorrer no olho tratado.
Entre em contato com o seu médicose tiver uma reação grave no olho.
Foram comunicados os seguintes efeitos adversos:
Muito frequentes(podem afetar mais de 1 de cada 10 pessoas)
- dor ocular
- hiperemia ocular (olho vermelho)
Frequentes(podem afetar até 1 de cada 10 pessoas)
- perfuração corneal (lesão da superfície da córnea)
- deficiência visual
- queratite ulcerosa (inflamação ou infecção da córnea)
- defeitos do epitélio corneal (defeitos da camada mais externa da córnea)
- infiltrados corneais (resposta imunitária a uma lesão corneal)
- queratite pontiaguda (pequenos desgastes na superfície do olho)
- lagrimeo (olhos lacrimejantes)
- hiperemia conjuntival (vermelhidão da conjuntiva)
- inflamação ocular
- irritação ocular
- fotofobia (sensibilidade desagradável do olho à luz)
- pápilas conjuntivais (vermelhidão, inchaço e irritação da face interna da pálpebra)
- prurido ocular (coceira nos olhos)
- secreção ocular
- inchaço ocular
- sensação de corpo estranho no olho
- molestias oculares
- olho seco
- conjuntivite (inflamação da camada mais externa do olho)
- infecção ocular
- agravamento do distúrbio (piora da doença)
- intolerância ao produto (hipersensibilidade ao medicamento)
- reações no local de aplicação, como dor
- reações no local de aplicação, como molestias
- reações no local de aplicação, como prurido (coceira)
- defeito epitelial persistente (perda persistente da camada mais externa da córnea após a lesão)
- toxicidade para vários agentes
- necessidade de transplante de córnea
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de AKANTIOR
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no envase após CAD. A data de validade é o último dia do mês que se indica do produto sem abrir.
Este medicamento não requer condições especiais de conservação.
Após abrir o sobrecartão, os envases unidose devem ser usados em um prazo de 28 dias. Após este período, os envases unidose não usados devem ser eliminados.
O conteúdo do envase unidose deve ser usado logo após abrir o envase e o conteúdo restante deve ser eliminado.
Os medicamentos não devem ser jogados nos deságues nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de AKANTIOR
- O princípio ativo é polihexanida. Cada mililitro de solução contém 0,8 mg de polihexanida.
- Os outros componentes são dihidrogenofosfato de sódio monohidratado, fosfato de disódio dodecahidratado, cloreto de sódio e água purificada.
AKANTIOR contém fosfatos (ver seção 2).
Aspecto do produto e conteúdo do envase
AKANTIOR colírio em solução em envase unidose (colírio) é uma solução transparente e incolor em um envase unidose.
Os envases unidose estão envasados em tiras seladas de 5 unidades que, por sua vez, estão incluídas em um sobrecartão de poliéster/alumínio/poliétileno e acondicionadas dentro de uma caixa.
Tamanhos de envases:
- 20 envases unidose
- 30 envases unidose
- envase múltiplo que contém 120 (4 envases de 30) envases unidose.
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
SIFI S.p.A.
Via Ercole Patti, 36
95025 Aci Sant'Antonio (CT)
Itália
Data da última revisão deste prospecto:
A informação detalhada deste medicamento está disponível na página web da Agência Europeia de Medicamentos: http://www.ema.europa.eu.
Pode acessar informação detalhada e atualizada sobre este medicamento escaneando com o seu telefone móvel (smartphone) ou dispositivo o código QR incluído no prospecto e na caixa. Também pode acessar esta informação no seguinte endereço de internet: https://qr.sifigroup.com/akantior/.
[código QR]
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSEForma farmacêutica: COLÍRIO, 50 mg/mlSubstância ativa: povidone-iodineRequer receita médicaForma farmacêutica: POMADA OFTÁLMICA, 20 mg/gSubstância ativa: bibrocatholFabricante: Brill Pharma S.L.Requer receita médicaForma farmacêutica: COLÍRIO, 5 mg/mlSubstância ativa: moxifloxacinFabricante: Tiedra Farmaceutica S.L.Requer receita médica
Alternativas a AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSE noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSE em Ucrania
Médicos online para AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSE
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de AKANTIOR 0,8 mg/ml COLÍRIO EM SOLUÇÃO EM EMBALAGEM UNIDOSE – sujeita a avaliação médica e regras locais.














