
ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE)
Pergunte a um médico sobre a prescrição de ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE)

Como usar ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE)
Introdução
Prospecto: informação para o utilizador
ADASUVE 9,1 mg pó para inalação (unidose)
loxapina
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou enfermeiro.
- Se experimentar efeitos adversos, consulte o seu médico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é ADASUVE e para que é utilizado
- O que precisa saber antes de começar a usar ADASUVE
- Como usar ADASUVE
- Possíveis efeitos adversos
- Conservação de ADASUVE
- Conteúdo do envase e informações adicionais
1. O que é ADASUVE e para que é utilizado
ADASUVE contém o princípio ativo loxapina, que pertence a um grupo de medicamentos denominados antipsicóticos. ADASUVE actua bloqueando certas substâncias químicas do cérebro (neurotransmissores), como a dopamina e a serotonina, de modo a produzir efeitos calmantes e alívio do comportamento agressivo.
ADASUVE é utilizado para tratar os sintomas agudos de agitação de leve a moderada que podem ocorrer em pacientes adultos com esquizofrenia ou transtorno bipolar. Estas são doenças que se caracterizam por sintomas tais como:
- (Esquizofrenia) ver, ouvir ou sentir coisas que não existem, desconfiança, crenças erróneas, fala e comportamento incoerente e indiferença emocional. As pessoas com esta doença também podem sentir-se deprimidas, culpadas, ansiosas ou tensas.
- (Transtorno Bipolar) sensação de “subidão”, com uma quantidade excessiva de energia, que precisa muito menos sono do que o normal, fala muito rápido com multitud de ideias e, às vezes, grande irritabilidade.
2. O que precisa saber antes de começar a usar ADASUVE
Não use ADASUVE
- se é alérgico à loxapina ou amoxapina;
- se tem sintomas de sibilancias ou dispneia;
- se tem problemas pulmonares como asma ou doença pulmonar obstructiva crónica (que o seu médico pode chamar “DPOC”).
Advertências e precauções
Consulte o seu médico ou enfermeiro antes de começar a usar ADASUVE para determinar se é adequado para si.
- ADASUVE pode produzir estreitamento das vias aéreas (broncoespasmo) e sibilancias, tos, opressão no peito ou falta de ar. Normalmente isto ocorre num prazo de 25 minutos desde a administração.
- O síndrome neuroléptico maligno (SNM) é um conjunto de sintomas que podem ocorrer se está tomando antipsicóticos, incluído ADASUVE. Estes sintomas podem ser febre alta, rigidez muscular, frequência cardíaca ou pulso irregulares ou rápidos. O SNM pode produzir a morte. Não use ADASUVE de novo se sofreu um SNM.
- Os medicamentos antipsicóticos como ADASUVE podem produzir movimentos que pode não ser capaz de controlar, por exemplo gestos faciais, sacar a língua, bater ou morder os lábios, pestanejar depressa ou mover as pernas, braços ou dedos rapidamente. Se isto ocorrer, deve suspender o tratamento com ADASUVE.
- ADASUVE será utilizado com precaução em pacientes intoxicados ou com delírio.
Antes de tomar ADASUVE, notifique o seu médico ou enfermeiro:
- se tem ou teve problemas respiratórios como asma e outras doenças pulmonares crónicas, tais como bronquite ou enfisema.
- se tem ou teve problemas cardíacos ou acidente vascular cerebral
- se tem ou teve hipotensão ou hipertensão
- se tem ou teve crises (convulsões)
- se tem ou teve glaucoma (aumento da tensão ocular)
- se tem ou teve retenção de urina (esvaziamento incompleto da bexiga urinária)
- se já usou ADASUVE e apresentou sintomas de sibilancias ou dispneia
- se sofreu movimentos musculares ou oculares que não pode controlar, falta de coordenação, contração muscular constante ou sensação de inquietude ou se não pode estar quieto
- se é uma pessoa de idade avançada com demência (perda de memória e de outras capacidades mentais)
Crianças e adolescentes
Não se recomenda o uso de ADASUVE em crianças e adolescentes menores de 18 anos
Uso de ADASUVE com outros medicamentos
Informe o seu médico se está tomando ou tomou recentemente ou poderia ter que tomar qualquer outro medicamento, incluídos:
- adrenalina
- medicamentos para tratar um problema respiratório
- medicamentos que poderiam provocar convulsões (p. ex. clozapina, tricíclicos ou ISRS, tramadol, mefloquina)
- medicamentos para tratar o Parkinson
- lorazepam ou outros medicamentos de ação central (para tratar a ansiedade, a depressão, a dor ou para dormir) ou outros medicamentos que produzem sonolência
- drogas (ilegais)
- medicamentos como fluvoxamina, propranolol e enoxacina, e outros medicamentos que inibem uma enzima hepática denominada “CYP450 1A2.”
- medicamentos para tratar a esquizofrenia, a depressão ou a dor, porque pode apresentar maior risco de sofrer convulsões
O uso de ADASUVE e adrenalina combinados pode produzir hipotensão.
Uso de ADASUVE com álcool
Desde que ADASUVE afeta o sistema nervoso, deve evitar o consumo de álcool durante o tratamento com ADASUVE.
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico antes de utilizar este medicamento. Recomenda-se que as mulheres não amamentem durante um período de 48 horas após a administração de ADASUVE e que despejem o leite produzido durante esse período. Podem produzir os seguintes sintomas em bebês recém-nascidos, de mães que foram tratadas com medicamentos antipsicóticos no último trimestre de gravidez: tremores, rigidez e/ou fraqueza muscular, sonolência, agitação, problemas para respirar, e dificuldade na alimentação. Se o seu bebê apresentar algum desses sintomas, deve contactar o seu médico.
Condução e uso de máquinas
Não conduza nem use ferramentas nem máquinas após tomar ADASUVE até que saiba como lhe afeta, pois os possíveis efeitos adversos de ADASUVE são tonturas, sedação e sonolência.
3. Como usar ADASUVE
Use sempre este medicamento seguindo exatamente as instruções de administração indicadas pelo seu médico ou enfermeiro. Em caso de dúvida, consulte novamente o seu médico ou enfermeiro.
A dose inicial recomendada é de 9,1 mg. Após 2 horas, o seu médico pode prescrever-lhe uma segunda dose após considerar cuidadosamente o seu estado e pode reduzir a dose para 4,5 mg se o seu médico acredita que esta é uma dose mais adequada para tratar a sua condição.
ADASUVE deve ser usado sob a supervisão de um médico ou enfermeiro.
ADASUVE está indicado para uso por via inhalatória. Após o médico ou enfermeiro ter preparado ADASUVE, será pedido que pegue no dispositivo com a mão, que exhale, que introduza a boquilha na boca, que inhale o medicamento através do dispositivo e que contenha a respiração durante alguns segundos.
Se tomar mais ADASUVE do que deve
Se acredita que tomou mais ADASUVE do que acredita que é necessário, informe o médico ou o enfermeiro. Os pacientes que recebem mais ADASUVE do que devem experimentarão algum dos seguintes sintomas: cansaço ou sonolência extremos, problemas para respirar, hipotensão, irritação de garganta ou mau sabor de boca, movimentos musculares ou oculares que não pode controlar.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou enfermeiro.
4. Possíveis efeitos adversos
Assim como com todos os medicamentos, pode produzir efeitos adversos, embora não todas as pessoas os sofram.
Se experimentar algum dos seguintes efeitos adversos, consulte o seu médico imediatamente e deixe de tomar o medicamento:
- sintomas respiratórios, como sibilancias, tos, falta de ar ou opressão no peito, pois poderia significar que o medicamento está irritando as vias respiratórias (pouco frequente a menos que você sofra asma ou DPOC);
- tonturas ou desmaios, pois poderia significar que o medicamento está diminuindo a sua tensão arterial (pouco frequente);
- pioreira da agitação ou confusão, especialmente combinado com febre ou rigidez muscular (infrequente). Estes podem estar associados a uma condição grave denominada síndrome maligno neuroléptico (SMN)
Assim como, consulte com o seu médico se apresentar algum dos seguintes efeitos adversos que também podem ocorrer com outras formas deste medicamento:
Muito frequentes(podem afetar mais de 1 de cada 10 pessoas): mau sabor de boca ou sonolência.
Frequentes(podem afetar até 1 de cada 10 pessoas): tonturas, irritação de garganta, secura de boca ou cansaço
Pouco frequentes(podem afetar até 1 de cada 100 pessoas): movimentos musculares ou oculares que não pode controlar, falta de coordenação, contração muscular constante ou sensação de inquietude ou se não pode estar quieto.
Outros efeitos adicionais que podem estar relacionados com o uso a longo prazo de loxapina por via oral e que podem ser pertinentes para ADASUVE incluem desmaios ao levantar-se, aumento da frequência cardíaca, hipertensão, visão borrosa, secura de olhos e diminuição da urina.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de ADASUVE
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize ADASUVE após a data de validade que aparece na etiqueta. A data de validade é o último dia do mês que se indica.
Conservar no embalagem original até que se vá a usar com o fim de protegê-lo da luz e da humidade.
Não use ADASUVE se a bolsa está aberta ou rasgada ou se há sinais de danos físicos no medicamento.
Os medicamentos não devem ser jogados no lixo. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
O princípio ativo é a loxapina. Cada inhalador de dose única contém 10 mg de loxapina e dispensa 9,1 mg de loxapina.
Aspecto de ADASUVE e conteúdo do envase
ADASUVE 9,1 mg pó para inalação (unidose), consiste em um inhalador de plástico branco, descartável e de um só uso que contém loxapina. Cada inhalador está envasado em uma bolsa de alumínio selada. ADASUVE 9,1 mg é apresentado em uma caixa de 1 ou 5 inhaladores de uma dose.
Titular da autorização de comercialização
Ferrer Internacional, S.A.
Gran Vía Carlos III, 94
08028- Barcelona
Espanha
Fabricante
Ferrer Internacional, S.A.
Joan Buscalla, 1-9, 08173 Sant Cugat del Vallès
Barcelona, Espanha
Pode solicitar mais informações respeito a este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
BélgicaLituânia
Ferrer Internacional, S.A. AOP Orphan Pharmaceuticals AG LT
Tel: +34 93 600 37 00 Tel: +370 672 12222
??????Luxemburgo
AOP Orphan Pharmaceuticals AG BG Ferrer Internacional, S.A.
Tel: +35 988 6666096 Tel: +34 93 600 37 00
República ChecaHungria
AOP Orphan Pharmaceuticals AG CZ AOP Orphan Pharmaceuticals AG HU
Tel: +420 251 512 947 Tel: +36 1 3192633
DinamarcaMalta
Ferrer Internacional, S.A. Ferrer Internacional, S.A.
Tel: +34 93 600 37 00 Tel: +34 93 600 37 00
AlemanhaPaíses Baixos
Ferrer Deutschland GmbH Ferrer Internacional, S.A.
Tel: +49 (0) 2407 502311 0 Tel: +34 93 600 37 00
EstôniaNoruega
AOP Orphan Pharmaceuticals AG LT Ferrer Internacional, S.A.
Tel: +370 672 12222 Tel: +34 93 600 37 00
GréciaÁustria
Ferrer Galenica S.A. AOP Orphan Pharmaceuticals AG
Tel: +30 210 52 81 700 Tel: +43 1 5037244-0
EspanhaPolônia
Ferrer Farma, S.A. AOP Orphan Pharmaceuticals S.A. PL
Tel: +34 93 600 37 00 Tel: +48 22 5424068
FrançaPortugal
Ferrer Internacional, S.A. Ferrer Portugal, S.A.
Tel: +34 93 600 37 00 Tel: +351 214449600
CroáciaRomênia
AOP Orphan Pharmaceuticals AG Galenica S.A.
Tel: +43 1 5037244-0 Tel: +30 210 52 81 700
IrlandaEslovênia
Ferrer Internacional, S.A. AOP Orphan Pharmaceuticals AG
Tel: +34 93 600 37 00 Tel: +43 1 5037244-0
IslândiaEslováquia
Ferrer Internacional, S.A. AOP Orphan Pharmaceuticals AG SK
Tel: +34 93 600 37 00 Tel: +421 31 5502271
Itália Angelini S.p.A. Tel: +39 06 780531 | Finlândia Ferrer Internacional, S.A. Tel: +34 93 600 37 00 |
Chipre Thespis Pharmaceutical Ltd Tel: +357 22 67 77 10 | Suécia Ferrer Internacional, S.A. Tel: +34 93 600 37 00 |
Letônia AOP Orphan Pharmaceuticals AG LT Tel: +370 672 12222 | Reino Unido Ferrer Internacional, S.A. Tel: +34 93 600 37 00 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Europeia de Medicamentos: http://www.ema.europa.eu.
Esta informação está destinada apenas a profissionais do setor sanitário:
Leia todas as instruções antes de utilizar este medicamento. Ver o RCP para mais informações.
Familiarize-se com ADASUVE:As imagens seguintes mostram os elementos importantes de ADASUVE.
 boquilha
boquilha
pó para inalação, loxapina |
luz indicadora
pestaña
- ADASUVE está envasado em uma bolsa selada.
- Quando ADASUVE é retirado da bolsa, a luz indicadora está apagada.
- A luz indicadora se acende (verde) quando se retira a pestaña. O inhalador está pronto para usar.
- A luz indicadora se apaga automaticamente de novo quando se tem inalado o medicamento. Leia os 5 passos seguintes antes de administrar ADASUVE a um paciente.
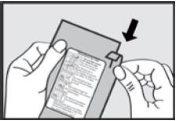
-{}- 1. Abrir a bolsa
Não abra a bolsa até que se vá a usar.Rasgue a bolsa de alumínio e retire o inhalador do seu embalagem.
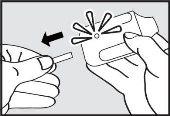
- Tirar da pestaña.
Tire forte da pestaña de plástico desde a parte posterior do inhalador. Se acenderá a luz verde, que indica que o inhalador está pronto para usar.
Use dentro dos primeiros 15 minutos após retirar a pestaña (ou até que a luz verde se apague) para evitar a desativação automática do inhalador.
Dê instruções ao paciente para que:
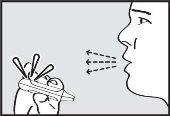
- Exhale
Mantenha o inhalador longe da boca e exhale completamente para esvaziar os pulmões.
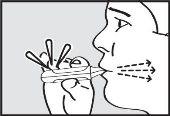
- Inhale
Inhale através da boquilha com uma inspiração profunda e contínua.
IMPORTANTE: Verifique que a luz verde se apaga após a inalação.
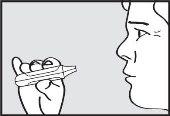
- Contenha a respiração
Retire a boquilha da boca e contenha a respiração durante alguns segundos.
NOTA: Se a luz verde continuar acesa após o paciente ter inalado, indique ao paciente que repita os passos 3 a 5.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE)Forma farmacêutica: INALAÇÃO PULMONAR, 9,1 mgSubstância ativa: loxapineFabricante: Ferrer Internacional S.A.Requer receita médicaForma farmacêutica: COMPRIMIDO, 100 mgSubstância ativa: clozapineFabricante: Aristo Pharma GmbhRequer receita médicaForma farmacêutica: COMPRIMIDO, 200 mgSubstância ativa: clozapineFabricante: Aristo Pharma GmbhRequer receita médica
Alternativas a ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE) noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE) em Ukraine
Médicos online para ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE)
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ADASUVE 9,1 mg PÓ PARA INALAÇÃO (UNIDOSE) – sujeita a avaliação médica e regras locais.










