

Scopolamine butylbromide Kalceks

Zapytaj lekarza o receptę na Scopolamine butylbromide Kalceks

Jak stosować Scopolamine butylbromide Kalceks
Ulotka dołączona do opakowania: informacja dla użytkownika
Scopolamine butylbromide Kalceks, 20 mg/ml, roztwór do wstrzykiwań
Hyoscini butylbromidum
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest Scopolamine butylbromide Kalceks i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Scopolamine butylbromide Kalceks
- 3. Jak stosować Scopolamine butylbromide Kalceks
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Scopolamine butylbromide Kalceks
- 6. Zawartość opakowania i inne informacje
1. Co to jest Scopolamine butylbromide Kalceks i w jakim celu się go stosuje
Scopolamine butylbromide Kalceks zawiera substancję czynną hioscyny butylobromek. Należy on do
grupy leków nazywanej „rozkurczowymi”. Leki te zmniejszają napięcie (stany skurczowe) narządów
wewnętrznych i związany z nim ból spastyczny.
Ten lek jest stosowany w łagodzeniu skurczów mięśni gładkich przewodu pokarmowego i układu
moczowo-płciowego (żołądka, jelit, dróg żółciowych, trzustki i dróg moczowych).
Scopolamine butylbromide Kalceks może być również stosowany w diagnostycznych procedurach
medycznych.
2. Informacje ważne przed zastosowaniem leku Scopolamine butylbromide Kalceks
Kiedy nie stosować leku Scopolamine butylbromide Kalceks
- jeśli pacjent ma uczulenie na hioscyny butylobromek lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
- jeśli pacjent ma jaskrę (choroba oczu);
- jeśli pacjent ma rozrost gruczołu krokowego i odczuwa trudności lub ból podczas oddawania moczu;
- jeśli pacjent ma zaburzenia drożności jelit;
- jeśli u pacjenta występuje nieprawidłowo powiększone jelito (rozszerzenie okrężnicy);
- jeśli pacjent ma przyspieszony rytm serca;
- jeśli u pacjenta występuje schorzenie nazywane „ myasthenia gravis” (charakteryzujące się skrajnym osłabieniem mięśni).
Nie należy podawać zastrzyku z hioscyny butylobromkiem do mięśnia, jeśli pacjent przyjmuje leki
zapobiegające tworzeniu się zakrzepów krwi (leki rozrzedzające krew), ponieważ mogą wystąpić
krwiaki (siniaki).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania tego leku należy omówić to z lekarzem, farmaceutą lub pielęgniarką:
- jeśli u pacjenta występuje ból brzucha o nieznanej przyczynie, który utrzymuje się lub nasila, lub występuje z gorączką, nudnościami, wymiotami, zmianami w wypróżnianiu, tkliwością brzucha, niskim ciśnieniem krwi, uczuciem osłabienia lub krwią w stolcu
- jeśli jego jelita nie pracują już prawidłowo (atonia jelitowa)
- jeśli pacjent ma stan zapalny przełyku związany z refluksem (gdy kwas solny cofa się z żołądka i dostaje się do przełyku)
- jeśli u pacjenta występuje ciężkie zapalenie jelita grubego, które często nawraca (wrzodziejące zapalenie jelita grubego)
- jeśli pacjent ma zaburzoną czynność wątroby lub nerek
- jeśli u pacjenta występuje nadczynność tarczycy (jego tarczyca wytwarza zbyt dużo hormonów tarczycy)
- jeśli u pacjenta występuje przewlekłe zapalenie oskrzeli (zapalenie oskrzelików).
Pacjent powinien natychmiast zgłosić się do lekarza, jeśli po wstrzyknięciu hioscyny butylobromku
wystąpi bolesne, zaczerwienie oka z utratą wzroku. Może to świadczyć o podwyższonym ciśnieniu
wewnątrz oka z powodu nierozpoznanej dotąd, i przez to nieleczonej, jaskry z wąskim kątem
przesączania.
Po wstrzyknięciu hioscyny butylobromku obserwowano reakcje alergiczne (patrz punkt 4). Dlatego,
po wstrzyknięciu hioscyny butylobromku pacjent będzie monitorowany i w przypadku wystąpienia
takich reakcji odpowiednio leczony.
Scopolamine butylbromide Kalceks a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować. To dotyczy też leków
przyjmowanych bez recepty i leków ziołowych.
W szczególności, należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje którykolwiek
z poniższych leków:
- leki przeciwdepresyjne zwane „trójpierścieniowymi lekami przeciwdepresyjnymi” lub „czteropierścieniowymi lekami przeciwdepresyjnymi”,
- leki stosowane w leczeniu alergii (leki przeciwhistaminowe),
- leki stosowane w leczeniu chorób psychicznych,
- leki stosowane w leczeniu niewydolności serca lub astmy (beta-mimetyki),
- leki stosowane w leczeniu zaburzeń rytmu serca (chinidyna lub dyzopiramid),
- amantadyna (lek stosowany w leczeniu choroby Parkinsona),
- leki stosowane w leczeniu zaburzeń oddychania (takie jak tiotropium, ipratropium, leki atropinopodobne),
- metoklopramid (lek stosowany w leczeniu nudności, wymiotów lub zaburzeń żołądkowo-jelitowych).
Jeśli pacjent nie jest pewien, czy którekolwiek z powyższych go dotyczy, należy porozmawiać
z lekarzem lub farmaceutą przed zastosowaniem tego leku.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed zastosowaniem tego leku.
Ciąża
Dane dotyczące stosowania leku u kobiet w ciąży i karmiących piersią są ograniczone. Dlatego ze
względów bezpieczeństwa nie zaleca się stosowania tego leku w okresie ciąży. W okresie ciąży lek
może być stosowany wyłącznie na zlecenie lekarza, który oceni stosunek korzyści do ryzyka.
Karmienie piersią
W okresie karmienia piersią lek może być stosowany wyłącznie na zlecenie lekarza, który oceni
stosunek korzyści do ryzyka.
Prowadzenie pojazdów i obsługiwanie maszyn
U niektórych pacjentów po leczeniu tym lekiem mogą wystąpić zaburzenia wzroku lub zawroty
głowy. W przypadku wystąpienia powyższych objawów należy poczekać, aż wzrok wróci do normy
lub ustąpią zawroty głowy przed rozpoczęciem prowadzenia pojazdów lub obsługiwania maszyn.
Scopolamine butylbromide Kalceks zawiera sód
Lek zawiera mniej niż 1 mmol (23 mg) sodu na dawkę, to znaczy lek uznaje się za „wolny od sodu”.
3. Jak stosować Scopolamine butylbromide Kalceks
Scopolamine butylbromide Kalceks będzie podawany pacjentowi przez lekarza lub pielęgniarkę
w powolnym wstrzyknięciu dożylnym, domięśniowym lub podskórnym. Dawkowanie ustali lekarz.
Tego leku nie należy stosować w sposób ciągły, codziennie lub przez dłuższy czas bez zbadania
przyczyny bólu brzucha.
Dorośli i dzieci wieku powyżej 12 lat
Zalecana dawka to 20 40 mg (1 2 ampułki) kilka razy na dobę. Maksymalna dawka dobowa to
100 mg (5 ampułek).
Stosowanie u dzieci
W ciężkich przypadkach, u niemowląt i dzieci może być stosowana dawka 0,3-0,6 mg/kg masy ciała
kilka razy na dobę. Nie należy przekraczać maksymalnej dawki dobowej 1,5 mg/kg masy ciała.
Zastosowanie większej niż zalecana dawki leku Scopolamine butylbromide Kalceks
Jeśli pacjent podejrzewa, że podano zbyt dużo leku, powinien natychmiast skonsultować się
z lekarzem lub pielęgniarką. Mogą wystąpić następujące objawy: suchość w ustach, zaczerwienienie
skóry, trudności w oddawaniu moczu, przyspieszenie akcji serca i zaburzenia widzenia.
Pominięcie zastosowania leku Scopolamine butylbromide Kalceks
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki. Kolejną dawkę pacjent
otrzyma tylko wtedy, gdy jest to wymagane ze względu na stan zdrowia.
Przerwanie stosowania leku Scopolamine butylbromide Kalceks
Lekarz zadecyduje o podaniu tego leku w postaci zastrzyku tylko w stanach ostrych. Jeśli konieczne
będzie kontynuowanie leczenia, lekarz zaleci stosowanie hioscyny butylobromku w tabletkach.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się
do lekarza lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Wiele z wymienionych działań niepożądanych można przypisać antycholinergicznym właściwościom
butylobromku hioscyny. Antycholinergiczne działania niepożądane butylobromku hioscyny są zwykle
łagodne i przemijające.
Do określenia częstości występowania działań niepożądanych zastosowano następującą klasyfikację:
Bardzo często
mogą wystąpić u więcej niż 1 na 10 pacjentów
Często
mogą wystąpić u mniej niż 1 na 10 pacjentów
Niezbyt często
mogą wystąpić u mniej niż 1 na 100 pacjentów
Rzadko
mogą wystąpić u mniej niż 1 na 1 000 pacjentów
Bardzo rzadko
mogą wystąpić u mniej niż 1 na 10 000 pacjentów
Częstość nieznana
nie może być określona na podstawie dostępnych danych
Zaburzenia układu immunologicznego
Częstość nieznana: wstrząs anafilaktyczny (nagła, ciężka reakcja alergiczna objawiająca się
dusznością, niewydolnością krążenia krwi i obrzękiem, w tym przypadki zakończone zgonem),
reakcje anafilaktyczne, duszność, reakcje skórne (np. pokrzywka, wysypka, zaczerwienienie skóry,
swędzenie), inne reakcje nadwrażliwości.
Zaburzenia psychiczne
Częstość nieznana: splątanie u osób w podeszłym wieku, pobudliwość, drażliwość.
Zaburzenia oka
Często:zaburzenia akomodacji (skupienia) oka.
Częstość nieznana:rozszerzenie źrenic, zwiększone ciśnienie wewnątrz oka, zmniejszenie
wydzielania łez.
Zaburzenia serca
Często:przyspieszone tętno.
Częstość nieznana: kołatanie serca.
Zaburzenia naczyniowe
Często: zawroty głowy.
Częstość nieznana: obniżone ciśnienie krwi, zaczerwienienie skóry.
Zaburzenia układu oddechowego
Częstość nieznana: zagęszczenie wydzieliny oskrzelowej.
Zaburzenia żołądka i jelit
Często: suchość w jamie ustnej.
Częstość nieznana: zaparcia.
Zaburzenia skóry i tkanki podskórnej
Częstość nieznana: zaburzenie wydalania potu.
Zaburzenia nerek i dróg moczowych
Częstość nieznana: trudności w oddawaniu moczu.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce.
Działania niepożądane można również zgłaszać bezpośrednio do Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych będzie można zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać Scopolamine butylbromide Kalceks
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Brak specjalnych zaleceń dotyczących przechowywania leku.
Nie stosować tego leku po upływie terminu ważności zamieszczonym na pudełku tekturowym
i ampułce po: „Termin ważności (EXP)” i ampułce po: „EXP”. Termin ważności oznacza ostatni
dzień podanego miesiąca.
Okres ważności po otwarciu ampułki: Lek powinien zostać natychmiast zużyty.
Okres ważności po rozcieńczeniu: Wykazano stabilność chemiczną i fizyczną w ciągu 24 godzin
w temperaturze 25°C i w 2-8°C.
Z mikrobiologicznego punktu widzenia, o ile metoda otwierania/rozcieńczania nie wyklucza ryzyka
skażenia mikrobiologicznego, lek należy zużyć natychmiast. Jeśli nie zostanie zużyty natychmiast,
użytkownik ponosi odpowiedzialność za czas i warunki przechowywania przed użyciem.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera Scopolamine butylbromide Kalceks
- Substancją czynną jest hioscyny butylobromek. Każda ampułka (1 ml) zawiera 20 mg hioscyny butylobromku.
- Pozostałe składniki to sodu chlorek, kwas solny stężony (do ustalenia pH), sodu wodorotlenek (do ustalenia pH), woda do wstrzykiwań.
Jak wygląda Scopolamine butylbromide Kalceks i co zawiera opakowanie
Roztwór do wstrzykiwań (płyn do wstrzykiwań).
Przezroczysty, bezbarwny lub prawie bezbarwny roztwór wolny od widocznych cząstek.
Ampułki z bezbarwnego szkła typu I o pojemności 1 ml.
Ampułki zapakowane są w blistry z folii PVC. Blistry zapakowane są w tekturowe pudełko.
Wielkości opakowań: 5 lub 10 ampułek
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
AS KALCEKS
Krustpils iela 71E
LV-1057 Rīga
Łotwa
Tel.: +371 67083320
E-mail: [email protected]
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego pod następującymi nazwami:
Czechy
Butylskopolaminium bromid Kalceks
Austria
Butylscopolaminiumbromid Kalceks 20 mg/ml Injektionslösung
Belgia
Scopolamine butylbromide Kalceks 20 mg/ml solution injectable
Scopolamine butylbromide Kalceks 20 mg/ml oplossing voor injectie
Scopolamine butylbromide Kalceks 20 mg/ml Injektionslösung
Bułgaria
Scopolamine butylbromide Kalceks 20 мг/мл инжекционен разтвор
Francja
SCOPOLAMIE BUTYLBROMURE KALCEKS 20 mg/mL, solution injectable
Włochy
Scopolamina butilbromuro Kalceks
Łotwa
Hyoscine butylbromide Kalceks 20 mg/ml šķīdums injekcijām
Norwegia
Skopolaminbutylbromid Kalceks
Polska
Scopolamine butylbromide Kalceks
Portugalia
Butilescopolamina Kalceks
Słowacja
Scopolamine butylbromide Kalceks 20 mg/ml injekčný roztok
Hiszpania
Butilescopolamina Kalceks 20 mg/ml solución inyectable EFG
Szwecja
Hyoscine butylbromide Kalceks
Holandia
Scopolamine butylbromide Kalceks 20 mg/ml oplossing voor injectie
Data ostatniej aktualizacji ulotki: 10/2022
-----------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Sposób podawania
Do wstrzykiwań dożylnych, domięśniowych lub podskórnych.
Instrukcje dotyczące użytkowania i usuwania
Wyłącznie do jednorazowego użytku. Po otwarciu, wszelkie niewykorzystane resztki należy usunąć.
Produkt leczniczy powinien być sprawdzony wizualnie przed użyciem. Można podać tylko
przezroczysty i wolny od cząsteczek roztwór.
Może być rozcieńczany z dekstrozą lub 0,9% roztworem chlorku sodu do wstrzykiwań.
Instrukcja otwierania ampułki
- 1) Obrócić ampułkę kolorowym punktem w górę. Jeśli w górnej części ampułki znajduje się roztwór, należy delikatnie stuknąć palcem, aby przenieść cały roztwór do dolnej części ampułki.
- 2) Użyć obu rąk, aby otworzyć ampułkę; trzymając dolną część ampułki w jednej ręce, drugą ręką odłamać górną część ampułki w kierunku od kolorowego punktu (patrz obrazek poniżej).
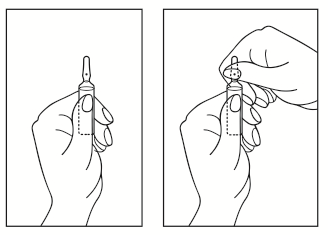
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie
z lokalnymi przepisami.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- ImporterAS Kalceks
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Scopolamine butylbromide KalceksPostać farmaceutyczna: Tabletki, 10 mgSubstancja czynna: butylscopolamineBez receptyPostać farmaceutyczna: Roztwór, 20 mg/mlSubstancja czynna: butylscopolamineProducent: Sopharma ADWymaga receptyPostać farmaceutyczna: Tabletki, 20 mgSubstancja czynna: butylscopolamineProducent: Delpharm ReimsBez recepty
Odpowiedniki Scopolamine butylbromide Kalceks w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Scopolamine butylbromide Kalceks – Ukraina
Odpowiednik Scopolamine butylbromide Kalceks – Hiszpania
Lekarze online w sprawie Scopolamine butylbromide Kalceks
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Scopolamine butylbromide Kalceks – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














