OMLYCLO 75 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA


Cómo usar OMLYCLO 75 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Omlyclo 75 mg solución inyectable en jeringa precargada
omalizumab
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Omlyclo y para qué se utiliza
- Qué necesita saber antes de empezar a usar Omlyclo
- Cómo usar Omlyclo
- Posibles efectos adversos
- Conservación de Omlyclo
- Contenido del envase e información adicional
1. Qué es Omlyclo y para qué se utiliza
Omlyclo contiene el principio activo omalizumab. Omalizumab es una proteína humana, similar a las proteínas naturales producidas por el organismo. Pertenece a una clase de medicamentos denominados anticuerpos monoclonales.
Omlyclo se utiliza para el tratamiento de:
- asma alérgica
- rinosinusitis crónica (inflamación de la nariz y de los senos) con pólipos nasales
Asma alérgica
Este medicamento se utiliza para prevenir que el asma empeore controlando los síntomas del asma alérgica grave en adultos, adolescentes y niños (a partir de 6 años de edad) que ya están recibiendo medicamentos para el asma, pero cuyos síntomas no se controlan adecuadamente con medicamentos tales como esteroides inhalados a dosis altas y beta agonistas inhalados.
Rinosinusitis crónica con pólipos nasales
Este medicamento se utiliza para tratar la rinosinusitis crónica con pólipos nasales en adultos (a partir de 18 años de edad) que están recibiendo corticosteroides intranasales (pulverización nasal con corticosteroides), pero cuyos síntomas no están bien controlados con estos medicamentos. Los pólipos nasales son pequeños crecimientos en el revestimiento de la nariz. Omlyclo ayuda a reducir el tamaño de los pólipos y mejora los síntomas incluyendo la congestión nasal, pérdida del sentido del olfato, mucosidad en la parte posterior de la garganta y secreción nasal.
Omlyclo actúa bloqueando una sustancia llamada inmunoglobulina E (IgE) que es producida por el organismo. La IgE interviene en un tipo de inflamación que juega un papel clave como causante del asma alérgica, la rinosinusitis crónica con pólipos nasales.
2. Qué necesita saber antes de empezar a usar Omlyclo
No use Omlyclo
- si es alérgico a omalizumab o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
Si cree que puede ser alérgico a cualquiera de los componentes, informe a su médico ya que no debe usar Omlyclo.
Advertencias y precauciones
Consulte a su médico antes de usar Omlyclo:
- si tiene problemas de riñón o hígado,
- si padece una alteración en la que su propio sistema inmune ataca partes de su propio organismo (enfermedad autoinmune),
- si va a viajar a una región donde las infecciones causadas por parásitos son comunes ya que Omlyclo puede disminuir su resistencia a dichas infecciones,
- si ha tenido una reacción alérgica grave (anafilaxia) previa, por ejemplo como consecuencia del uso de una medicina, una picadura de un insecto o por comida.
Omlyclo no trata los síntomas del asma agudo, como puede ser un ataque de asma repentino. Por lo tanto, Omlyclo no debe utilizarse para tratar esta clase de síntomas.
Omlyclo no está destinado para prevenir o tratar otras afecciones de tipo alérgico, como son reacciones alérgicas repentinas, síndrome de hiperinmunoglobulina E (trastorno inmune hereditario), aspergilosis (enfermedad del pulmón causada por un hongo), alergia alimentaria, eczema o fiebre del heno ya que Omlyclo no se ha estudiado en estas afecciones.
Vigile los signos de reacciones alérgicas y otros efectos adversos graves
Omlyclo puede ocasionar efectos adversos graves. Usted debe vigilar la aparición de signos de estos efectos mientras use Omlyclo. Busque asistencia médica de forma inmediata si nota algún signo que indique una reacción alérgica grave u otros efectos adversos graves. Esos signos se mencionan en “Efectos adversos graves” en la sección 4.
Antes de que usted se inyecte Omlyclo o de que lo haga otra persona distinta a un profesional sanitario, es importante que reciban formación de su médico sobre cómo reconocer los síntomas tempranos de reacciones alérgicas graves y de cómo actuar si se producen (ver sección 3,“Cómo usar Omlyclo”). La mayoría de las reacciones alérgicas graves ocurren durante las tres primeras dosis de Omlyclo.
Niños y adolescentes
Asma alérgica
Omlyclo no está recomendado para niños menores de 6 años de edad. Su uso en niños menores de 6 años de edad no se ha estudiado.
Rinosinusitis crónica con pólipos nasales
Omlyclo no está recomendado para niños y adolescentes menores de 18 años de edad. Su uso en pacientes menores de 18 años de edad no se ha estudiado.
Otros medicamentos y Omlyclo
Informe a su médico, farmacéutico o enfermero si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento.
Esto es especialmente importante si está utilizando:
- medicamentos para tratar una infección causada por un parásito, ya que Omlyclo puede reducir el efecto de sus medicamentos,
- corticosteroides inhalados y otros medicamentos para el asma alérgica.
Embarazo y lactancia
Si está embarazada, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes de utilizar este medicamento. Su médico comentará con usted los beneficios y riesgos potenciales del uso de este medicamento durante el embarazo.
Informe a su médico inmediatamente si queda embarazada mientras está siendo tratada con Omlyclo.
Omlyclo puede pasar a la leche materna. Si usted está dando el pecho o tiene intención de hacerlo, consulte a su médico antes de usar este medicamento.
Conducción y uso de máquinas
No es probable que Omlyclo afecte a su capacidad para conducir y usar máquinas.
3. Cómo usar Omlyclo
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico, farmacéutico o enfermero.
Cómo se usa Omlyclo
Omlyclo se usa como una inyección bajo la piel (conocida como inyección subcutánea).
Inyección de Omlyclo
- Usted y su médico decidirán si se va a inyectar usted mismo Omlyclo. Las tres primeras dosis se inyectarán siempre bajo la supervisión de un profesional sanitario (ver sección 2).
- Es importante haber recibido la formación adecuada sobre cómo inyectarse el medicamento antes de que lo haga usted mismo.
- El cuidador (por ejemplo los padres) puede ponerle la inyección de Omlyclo después de haber recibido la formación apropiada.
Para obtener instrucciones detalladas sobre como inyectar Omlyclo, ver “Instrucciones de uso de Omlyclo en jeringa precargada” al final de este prospecto.
Formación para reconocer reacciones alérgicas graves
Es también importante que no se inyecte Omlyclo a usted mismo hasta que su médico o enfermera no le hayan enseñado:
- cómo reconocer los signos y síntomas tempranos de reacciones alérgicas graves,
- qué hacer si los síntomas aparecen.
Para más información sobre los signos y síntomas tempranos de reacciones alérgicas graves, ver sección 4.
Cuánto se administrará
Su médico decidirá la cantidad de Omlyclo que necesita y la frecuencia de administración del mismo. Ello depende de su peso corporal y de los resultados de un análisis de sangre realizado antes de iniciar el tratamiento para determinar la concentración de IgE en su sangre.
Necesitará entre 1 y 4 inyecciones al mismo tiempo. Necesitará las inyecciones cada dos o cada cuatro semanas.
Continúe tomando su medicación actual para el asma y/o pólipos nasales mientras dure el tratamiento con Omlyclo. No interrumpa ninguna medicación para el asma y/o pólipos nasales sin consultarlo con su médico.
Es posible que no perciba una mejoría inmediata después de iniciar el tratamiento con Omlyclo. En pacientes con pólipos nasales los efectos se han observado 4 semanas después del inicio del tratamiento. En pacientes con asma, por lo general, deben transcurrir entre 12 y 16 semanas hasta que el medicamento surta todo su efecto.
Uso en niños y adolescentes
Asma alérgica
Omlyclo se puede usar en niños y adolescentes a partir de 6 años que ya estén recibiendo medicación para el asma, pero cuyos síntomas asmáticos no están bien controlados por medicamentos como dosis elevadas de esteroides inhalados y beta-agonistas inhalados. Su médico le informará qué cantidad de Omlyclo necesita su hijo y con qué frecuencia se le debe administrar. Esto dependerá del peso del niño y de los resultados obtenidos de los análisis de sangre realizados antes de iniciar el tratamiento para determinar la cantidad de IgE en su sangre.
No se espera que los niños (de 6 a 11 años de edad) se administren Omlyclo a ellos mismos. Sin embargo, si el médico lo considera conveniente, el cuidador puede administrarles la inyección de Omlyclo después de la formación adecuada.
Rinosinusitis crónica con pólipos nasales
Omlyclo no se debe usar en niños y adolescentes menores de 18 años de edad.
Si olvidó una dosis de Omlyclo
Si ha olvidado una visita, contacte con su médico u hospital tan pronto como sea posible para volver a programarla.
Si ha olvidado autoinyectarse una dosis de Omlyclo, inyéctesela tan pronto como lo recuerde. Después consulte con su médico para saber cuándo se deberá administrar la siguiente dosis.
Si interrumpe el tratamiento con Omlyclo
No interrumpa el tratamiento con Omlyclo a no ser que se lo indique su médico. La interrupción o finalización del tratamiento con Omlyclo puede causar una recidiva de sus síntomas.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los efectos adversos causados por Omlyclo son, por lo general, de leves a moderados pero ocasionalmente pueden ser graves.
Efectos adversos graves:
Busque atención médica inmediata si usted nota alguno de los signos de los siguientes efectos adversos:
Raros (pueden afectar hasta 1 de cada 1 000 pacientes)
- Reacciones alérgicas graves (incluida anafilaxia). Los síntomas pueden incluir erupción, picor, habones en la piel, hinchazón de la cara, labios, lengua, laringe (caja de voz), tráquea u otras partes del cuerpo, ritmo cardíaco rápido, mareo y ligera sensación de vahído, confusión, disnea, respiración jadeante o dificultad respiratoria, piel o labios azulados, colapso y pérdida de consciencia. Si tiene antecedentes de reacciones alérgicas graves (anafilaxia) no relacionados con Omlyclo, puede sufrir mayor riesgo de desarrollar una reacción alérgica grave después del uso de Omlyclo.
- Lupus eritematoso sistémico (LES). Los síntomas pueden incluir dolor muscular, dolor e hinchazón de las articulaciones, erupción, fiebre, pérdida de peso y fatiga.
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles)
- Síndrome de Churg-Strauss o síndrome hipereosinofílico. Los síntomas pueden incluir uno o más de los siguientes: hinchazón, dolor o erupción alrededor de los vasos sanguíneos o linfáticos, nivel elevado de un tipo específico de glóbulos blancos (eosinofilia marcada), empeoramiento de los problemas respiratorios, congestión nasal, problemas cardíacos, dolor, adormecimiento, hormigueo en los brazos y piernas.
- Recuento de plaquetas sanguíneas bajo con síntomas como sangrado o hematomas que se producen más fácilmente de lo normal.
- Enfermedad del suero. Los síntomas pueden incluir uno o más de los siguientes: dolor en las articulaciones con o sin inflamación o rigidez, erupción, fiebre, inflamación de los nódulos linfáticos, dolor muscular.
Otros efectos adversos incluyen:
Muy frecuentes (pueden afectar a más de 1 de cada 10 pacientes)
- fiebre (en niños)
Frecuentes (pueden afectar hasta 1 de cada 10 pacientes)
- reacciones en la zona de inyección que incluyen dolor, hinchazón, picor y enrojecimiento
- dolor en la parte superior del estómago
- dolor de cabeza (muy frecuente en niños)
- sensación de mareo
- dolor en las articulaciones (artralgia)
Poco frecuentes (pueden afectar hasta 1 de cada 100 pacientes)
- sensación de sueño o cansancio
- hormigueo o entumecimiento de manos o pies
- desmayo, disminución de la tensión arterial al sentarse o ponerse de pie (hipotensión postural), rubefacción
- dolor de garganta, tos, problemas respiratorios agudos
- sensación de mareo (nausea), diarrea, indigestión
- picor, habones, erupción, mayor sensibilidad de la piel al sol
- aumento de peso
- síntomas de tipo gripal
- brazos hinchados
Raros (pueden afectar hasta 1 de cada 1 000 pacientes)
- infección parasitaria
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles)
- dolor muscular e inflamación de las articulaciones
- pérdida de pelo
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Omlyclo
- Mantener este medicamento fuera de la vista y del alcance de los niños.
- No utilice este medicamento después de la fecha de caducidad que aparece en el etiquetado después de CAD/EXP. La fecha de caducidad es el último día del mes que se indica. El envase que contiene la jeringa precargada puede conservarse durante un total de 7 días a temperatura ambiente (25 °C) antes de usar.
- Conservar en el embalaje original para protegerlo de la luz.
- Conservar en nevera (entre 2 °C y 8 °C). No congelar.
- No utilizar ningún envase que esté dañado o muestre indicios de deterioro.
6. Contenido del envase e información adicional
Composición de Omlyclo
- El principio activo es omalizumab. Una jeringa de 0,5 ml de solución contiene 75 mg de omalizumab.
- Los demás componentes son L-hidrocloruro de arginina, L-hidrocloruro de histidina monohidrato, L-histidina, polisorbato 20 y agua para preparaciones inyectables.
Aspecto de Omlyclo y contenido del envase
Omlyclo solución inyectable se presenta como una solución de transparente a turbia, incolora a color amarillo parduzco claro en una jeringa precargada.
Omlyclo 75 mg solución inyectable está disponible en envases que contienen 1 jeringa precargada
Titular de la autorización de comercialización
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Hungría
Responsable de la fabricación
Nuvisan France SARL
2400, Route des Colles,
06410, Biot,
Francia
MIDAS Pharma GmbH
Rheinstrasse 49
55218 West Ingelheim Am Rhein
Rhineland-Palatinate
Alemania
Kymos S.L.
Ronda de Can Fatjó 7B
Parc Tecnològic del Vallès
08290 Cerdanyola Del Valles
Barcelona
España
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Celltrion Healthcare Belgium BVBA Tél/Tel: + 32 1 528 7418 | Lietuva Celltrion Healthcare Hungary Kft. Tel.: +36 1 231 0493 |
| Luxembourg/Luxemburg Celltrion Healthcare Belgium BVBA Tél/Tel: + 32 1 528 7418 |
Ceská republika Celltrion Healthcare Hungary Kft. Tel: +36 1 231 0493 | Magyarország Celltrion Healthcare Hungary Kft. Tel.: +36 1 231 0493 |
Danmark Celltrion Healthcare Denmark ApS Tlf: +45 3535 2989 | Malta Mint Health Ltd. Tel: +356 2093 9800 |
Deutschland Celltrion Healthcare Deutschland GmbH Tel: +49 303 464 941 50 | Nederland Celltrion Healthcare Netherlands B.V. Tel: + 31 20 888 7300 |
Eesti Celltrion Healthcare Hungary Kft. Tel: +36 1 231 0493 | Norge Celltrion Healthcare Norway AS [email protected] |
España CELLTRION FARMACEUTICA (ESPAÑA) S.L. Tel: +34 910 498 478 | Österreich Astro-Pharma GmbH Tel: +43 1 97 99 860 |
Ελλáδα ΒΙΑΝΕΞ Α.Ε. Τηλ: +30 210 8009111 - 120 | Polska Celltrion Healthcare Hungary Kft. Tel.: +36 1 231 0493 |
France Celltrion Healthcare France SAS Tél.: +33 (0)1 71 25 27 00 | Portugal CELLTRION PORTUGAL, UNIPESSOAL LDA Tel: +351 21 936 8542 |
Hrvatska Oktal Pharma d.o.o. Tel: +385 1 6595 777 | România Celltrion Healthcare Hungary Kft. Tel: +36 1 231 0493 |
Ireland Celltrion Healthcare Ireland Limited Tel: +353 1 223 4026 | Slovenija OPH Oktal Pharma d.o.o. Tel.: +386 1 519 29 22 |
Ísland Celltrion Healthcare Hungary Kft. Sími: +36 1 231 0493 | Slovenská republika Celltrion Healthcare Hungary Kft. Tel: +36 1 231 0493 |
Italia Celltrion Healthcare Italy S.R.L. Tel: +39 0247927040 | Suomi/Finland Celltrion Healthcare Finland Oy. Puh/Tel: +358 29 170 7755 |
Κúπρος C.A. Papaellinas Ltd Τηλ: +357 22741741 | Sverige Celltrion Sweden AB [email protected] |
Latvija Celltrion Healthcare Hungary Kft. Talr.: +36 1 231 0493 |
Fecha de la última revisión deeste prospecto:
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu
INSTRUCCIONES DE USO DE OMLYCLO JERINGA PRECARGADA
Lea y siga las instrucciones de uso que se facilitan con Omlyclo jeringa precargada antes de empezar a usarla y cada vez que obtenga un recambio. Pueden contener información nueva.
Esta información no sustituye a la consulta con su profesional sanitario sobre su enfermedad o tratamiento.
Los niños (de 6 a menos de 12 años de edad) no deben autoinyectarse Omlyclo jeringa precargada; sin embargo, si el profesional sanitario lo considera apropiado, un cuidador puede administrarles la inyección después de haber recibido la formación adecuada.
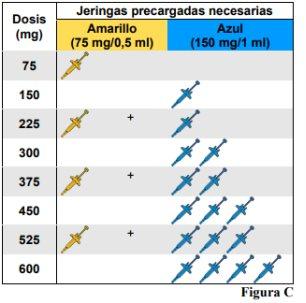
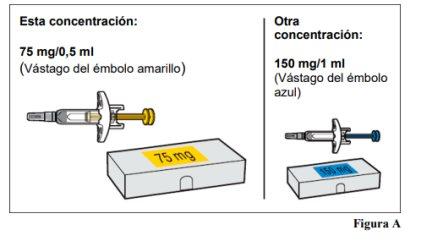
Omlyclo jeringa precargada está disponible en 2 concentraciones(véase la Figura A). Estas instrucciones se deben seguir para la concentración de 75 mg/0,5 ml. El tipo de jeringa precargada que reciba dependerá de la dosis prescrita por su profesional sanitario (véase la Figura C: Tabla de dosificación). Compruebe la etiqueta del envase y el color del vástago del émbolo para asegurarse de que la concentración es la correcta.
Información importante de seguridad
- Mantenga la jeringa precargada fuera de la vista y del alcance de los niños. La jeringa precargada contiene piezas pequeñas.
- Noabra el envase precintado hasta que vaya a utilizar la jeringa precargada.
- Noutilice la jeringa precargada si el precinto del envase o el precinto de la bandeja de plástico están rotos, ya que puede que no sea seguro utilizarla.
- Nodeje nunca la jeringa precargada en un lugar donde otras personas puedan manipularla.
- Noagite la jeringa precargada.
- Noretire el capuchón hasta justo antes de administrar la inyección.
- No se puede reutilizar la jeringa precargada. Deseche la jeringa precargada usada en un recipiente para objetos punzocortantes inmediatamente después de utilizarla (véase el paso 13. Desechar la jeringa precargada).
Conservación de la jeringa precargada
- Conserve la jeringa precargada en la nevera entre 2 °C y 8 °C. Conserve este medicamento cerrado dentro de su envase para protegerlo de la luz.
- Nocongele la jeringa precargada.
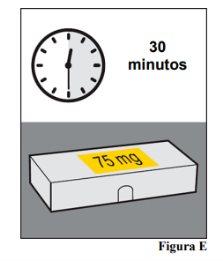
- Recuerde sacar la jeringa precargada de la nevera y deje que alcance la temperatura ambiente (25 °C), unos 30 minutos, antes de prepararla para la inyección. Deje la jeringa precargada en el envase para protegerla de la luz.
- El tiempo de conservación de la jeringa precargada a temperatura ambiente (25 °C) antes de su uso no debe sobrepasar los 7 días.
- Noutilice la jeringa precargada después de la fecha de caducidad que aparece en el envase y en la etiqueta de la jeringa precargada. Si ha caducado, devuelva todo el envase a la farmacia.
- Noutilice la jeringa precargada si se le ha caído o está visiblemente dañada.
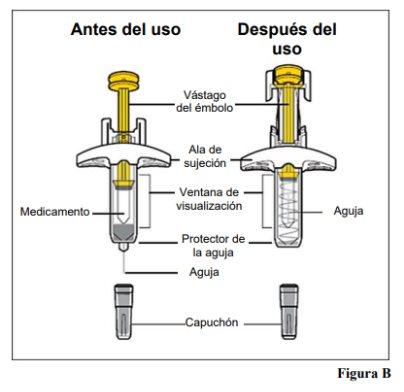
Partes de la jeringa precargada (véase laFigura B)
Preparación para la inyección
|
inyección 1.a. Prepare una superficie limpia y plana, como una mesa o un mostrador, en una zona bien iluminada. 1.b. Saque de la nevera el(los) envase(s) que contiene(n) la(s) jeringa(s) precargada(s) necesaria(s) para administrar la dosis que le han prescrito. Nota: Dependiendo de la dosis que le haya prescrito su profesional sanitario, puede que deba preparar una o más jeringas precargadas e inyectarse el contenido de todas ellas. La siguiente tabla muestra cuántas inyecciones de cada concentración son necesarias para la dosis prescrita (véase la Figura C: Tabla de dosificación). 1.c. Asegúrese de que dispone de los siguientes materiales:
precargada No incluido en el envase:
punzocortantes |
|
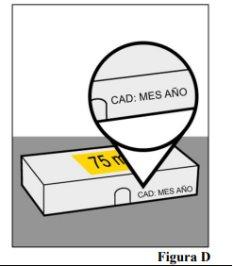
el envase (véase laFigura D).
caducidad ha pasado. Si la fecha de caducidad ha pasado, devuelva todo el envase a la farmacia. |
|
3.a. Deje el envase sin abrirque contiene la jeringa precargada a temperatura ambiente (25 °C) durante 30 minutos para que se caliente (véase la Figura E).
utilizando fuentes de calor como agua caliente o un microondas.
alcanza la temperatura ambiente, la inyección podría resultar incómoda y dificultar el empuje del vástago del émbolo. |
|
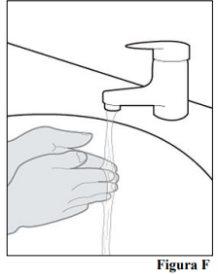
4.a. Lávese las manos con agua y jabón y séqueselas bien (véase la Figura F). |
|
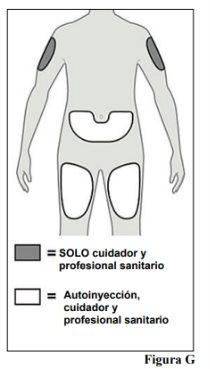
Figura G) 5.a. Puede inyectarse en:
excepto en los 5 cm alrededor del ombligo.
superior del brazo si usted es un cuidador o un profesional sanitario.
lunares, cicatrices, moratones o zonas en las que la piel esté sensible, enrojecida, dura o si hay grietas en la piel.
través de la ropa. 5.b. Elija un lugar de inyección diferente para cada nueva inyección a una distancia mínima de 2,5 cm de la zona utilizada para la última inyección. |
|
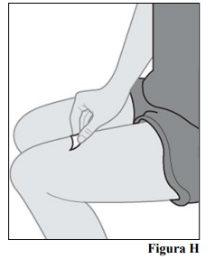
6.a. Limpie el lugar de inyección con una toallita empapada en alcohol realizando un movimiento circular (véase la Figura H). 6.b. Deje que la piel se seque antes de inyectar.
lugar de inyección antes de administrar la inyección |
|
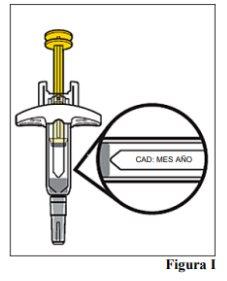
7.a Abra el envase. Agarre el cuerpo de la jeringa precargada para levantarla de la bandeja. 7.b Examine la jeringa precargada y asegúrese de que tiene el medicamento (Omlyclo) y la dosis correctos. 7.c Observe la jeringa precargada y asegúrese de que no esté agrietada ni dañada. 7.d Compruebe la fecha de caducidad en la etiqueta de la jeringa precargada (véase la Figura I).
caducidad ha pasado. Nota: Si la fecha de caducidad no es visible en la ventana de visualización, puede girar el cilindro interior de la jeringa precargada hasta que la fecha de caducidad sea visible. |
|
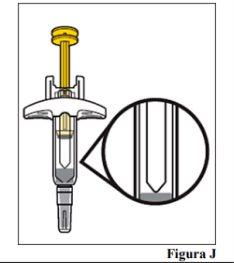
8.a. Observe el medicamento y confirme que el líquido es de transparente a turbio, de incoloro a amarillo parduzco claro, y que no tiene partículas (véase la Figura J).
si el líquido presenta cambios de color, está claramente turbio o contiene partículas.
aire en el líquido. Esto es normal. |
Administración de la inyección
|
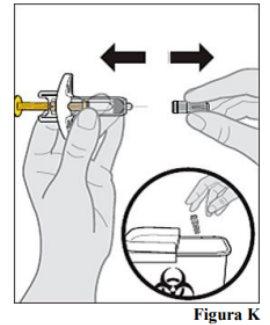
9.a. Sujete la jeringa precargada por el cuerpo con una mano. Con la otra mano, tire suavemente del capuchón para retirarlo.
mientras retira el capuchón.
líquido en la punta de la aguja. Esto es normal. 9.b. Deseche el capuchón inmediatamente en un recipiente para objetos punzocortantes (véase el paso 13. Desechar la jeringa precargaday la Figura K).
la jeringa precargada.
esté preparado para administrar la inyección.
contrario, podría pincharse con la aguja. |
|
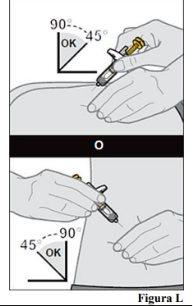
lugar de inyección. 10.a. Pellizque suavemente con una mano un pliegue de piel en el lugar de inyección. Nota:Es importante pellizcar la piel para asegurarse de que se inyecta bajo la piel (en la zona grasa) pero no más profundamente (en el músculo). 10.b. Con un movimiento rápido y tipo «dardo», inserte la aguja completamente en el pliegue de piel en un ángulo de 45 a 90 grados (véase la Figura L).
mientras inserta la aguja en la piel. |
|
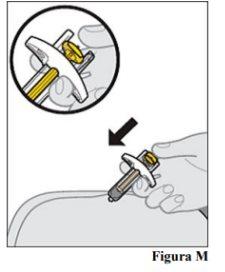
11.a. Una vez insertada la aguja, suelte el pellizco de piel. 11.b. Empuje lentamente el vástago del émbolo hacia abajohasta que se inyecte toda la dosis del medicamento y la jeringa esté vacía (véase la Figura M).
jeringa precargada una vez iniciada la inyección.
completamente presionado, el protector de la aguja no se extenderá para cubrir la aguja cuando se retire. |
|
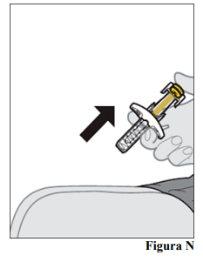
lugar de inyección 12.a. Una vez que la jeringa precargada esté vacía, levante lentamente el pulgar del vástago del émbolo hasta que la aguja esté completamente cubierta por el protector de la aguja (véase la Figura N).
proceda con cuidado para desechar la jeringa (véase el paso 13. Desechar la jeringa precargada).
(véase el paso 14. Cuidados del lugar de inyección).
medicamento con la piel, lave con agua la zona que ha estado en contacto con el medicamento.
precargada.
|
Después de lainyección
|
13.a. Coloque la jeringa precargada usada en un recipiente para objetos punzocortantes inmediatamente después de usarla (véase la Figura O).
precargada en la basura doméstica. Si no dispone de un recipiente para objetos punzocortantes, puede utilizar un recipiente doméstico que se pueda cerrar y que sea resistente a los pinchazos. Por su seguridad y su salud y la de los demás, las agujas y las jeringas usadas no deben reutilizarse nunca. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente. |
14.a. Si se produce sangrado, trate el lugar de la inyección presionando suavemente, sin frotar, con una torunda de algodón o gasa en el lugar y aplique un apósito adhesivo si es necesario. |
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a OMLYCLO 75 MG SOLUCION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 150 mgPrincipio activo: OmalizumabFabricante: Celltrion Healthcare Hungary Kft.Requiere recetaForma farmacéutica: INYECTABLE, 150 mgPrincipio activo: OmalizumabFabricante: Novartis Europharm LimitedRequiere recetaForma farmacéutica: INYECTABLE, 150 mgPrincipio activo: OmalizumabFabricante: Novartis Europharm LimitedRequiere receta
Médicos online para OMLYCLO 75 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de OMLYCLO 75 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes