
Tobradex
Consulta con un médico sobre la receta médica de Tobradex

Cómo usar Tobradex
HOJA DE INSTRUCCIONES DEL PACIENTE: INFORMACIÓN SOBRE EL MEDICAMENTO
Atención: conserve esta hoja de instrucciones, la información en el embalaje primario está en un idioma extranjero.
Tobradex
(3 mg + 1 mg)/ml, gotas para los ojos, suspensión
Tobramicina + Dexametasona
Es importante leer atentamente el contenido de esta hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a su médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones
- 1. Qué es Tobradex y para qué se utiliza
- 2. Información importante antes de usar Tobradex
- 3. Cómo usar Tobradex
- 4. Posibles efectos adversos
- 5. Cómo conservar Tobradex
- 6. Contenido del embalaje y otra información
1. Qué es Tobradex y para qué se utiliza
Tobradex se utiliza para tratar enfermedades inflamatorias de los ojos que pueden estar acompañadas de
infección. La inflamación del ojo puede ser el resultado de una cirugía ocular, infección y puede ser causada por la presencia de un cuerpo extraño o lesión en el ojo.
Tobradex es un medicamento combinado que contiene un componente antibacteriano y
corticosteroide. Los corticosteroides (en este caso, dexametasona) se utilizan para prevenir y reducir la inflamación en los ojos. El componente antibacteriano del medicamento (tobramicina) actúa sobre muchas especies de bacterias patógenas que infectan el ojo.
La indicación para usar Tobradex es la prevención y el tratamiento de la inflamación y la prevención de infecciones relacionadas con la cirugía de cataratas en adultos y niños mayores de 2 años.
2. Información importante antes de usar Tobradex
Cuándo no usar Tobradex
- si el paciente es alérgico a la dexametasona, tobramicina o cualquier otro componente de este medicamento (enumerados en el punto 6) o si el paciente tiene:
- inflamación de la córnea causada por el virus del herpes;
- inflamación de la córnea causada por el virus de la varicela, el sarampión o otras enfermedades virales de la córnea o la conjuntiva;
- tuberculosis ocular;
- infección fúngica ocular o infecciones parasitarias oculares no tratadas;
- infecciones oculares purulentas no tratadas;
- si al paciente se le ha extirpado un cuerpo extraño de la córnea y no hay signos de complicaciones.
Advertencias y precauciones
- Si después de usar Tobradex, el paciente experimenta reacciones alérgicas, debe suspender el tratamiento y consultar inmediatamente a un médico (véase el punto 4). Los síntomas de hipersensibilidad pueden variar en gravedad: desde picazón o enrojecimiento localizado hasta reacciones alérgicas graves (anafilaxia) o reacciones cutáneas graves. Estas reacciones alérgicas pueden ocurrir con el uso de otros antibióticos tópicos o sistémicos de la misma clase (aminoglucósidos).
- Si el paciente experimenta un empeoramiento de los síntomas o una recurrencia repentina de los síntomas de la enfermedad, debe consultar a un médico. Durante el uso de este medicamento, el paciente puede ser más susceptible a infecciones oculares.
- Si el paciente está usando otros antibióticos, incluyendo aquellos que se toman por vía oral, debe consultar a un médico.
- Si el paciente tiene o sospecha que tiene miastenia o enfermedad de Parkinson, debe consultar a un médico. Los antibióticos de esta clase pueden aumentar la debilidad muscular.
- Si el paciente usa Tobradex durante un período prolongado, puede experimentar:
- aumento de la susceptibilidad a infecciones oculares,
- aumento de la presión intraocular,
- desarrollo de cataratas,
- desarrollo del síndrome de Cushing debido a la absorción del medicamento en la sangre. Debe consultar a un médico si experimenta hinchazón y aumento de peso, especialmente en el tronco y la cara, ya que estos son los primeros síntomas de esta enfermedad. La supresión de la función suprarrenal puede ocurrir después de la suspensión del uso prolongado o intensivo de Tobradex. Debe consultar a un médico antes de suspender el tratamiento. Este riesgo es especialmente importante en niños y pacientes que están tomando ritonavir o cobicistat.
- Durante el uso de Tobradex, debe controlar regularmente la presión intraocular; debe consultar a un médico. Esto es especialmente importante en niños, ya que el riesgo de desarrollar hipertensión ocular inducida por corticosteroides puede ser mayor en niños y puede ocurrir más rápidamente que en adultos. Especialmente en niños y adolescentes, debe consultar a un médico. El riesgo de hipertensión ocular inducida por corticosteroides y el desarrollo de cataratas también es mayor en pacientes con otras enfermedades (por ejemplo, pacientes con diabetes).
- Los medicamentos esteroides tópicos pueden causar una curación retardada de las heridas oculares. Los medicamentos antiinflamatorios no esteroides (AINE) tópicos pueden ralentizar y retrasar el proceso de curación. El uso concomitante de AINE y medicamentos esteroides puede aumentar el riesgo de problemas de curación ocular.
- Si el paciente tiene una enfermedad que causa adelgazamiento de los tejidos oculares, debe consultar a un médico o farmacéutico.
- Si el paciente experimenta una úlcera corneal persistente mientras usa Tobradex, debe consultar a un médico lo antes posible, ya que puede ser un signo de infección fúngica ocular.
Si el paciente experimenta visión borrosa u otros trastornos de la visión, debe consultar a un médico.
Tobradex y otros medicamentos
Debe informar a su médico sobre todos los medicamentos que está tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar.
Debe informar a su médico especialmente si está tomando AINE.
El uso concomitante de un medicamento esteroide y un AINE puede causar problemas de curación ocular.
Si el paciente está tomando otros medicamentos para los ojos, debe esperar al menos 5 minutos entre las administraciones de los diferentes medicamentos. Los ungüentos para los ojos deben aplicarse al final.
Debe informar a su médico sobre el uso de ritonavir o cobicistat, ya que estos medicamentos pueden aumentar la concentración de dexametasona en la sangre.
Embarazo y lactancia
Si la paciente está embarazada o en período de lactancia, cree que puede estar embarazada o planea tener un hijo, debe consultar a un médico antes de usar este medicamento.
No se recomienda el uso de Tobradex durante el embarazo y la lactancia.
Conducción de vehículos y uso de máquinas
Las gotas oculares de Tobradex no tienen un efecto significativo o tienen un efecto mínimo en la capacidad de conducir vehículos o usar máquinas.
Después de la administración de Tobradex, la visión puede ser borrosa durante un tiempo. No debe conducir vehículos ni usar máquinas hasta que este efecto desaparezca.
Tobradex contiene cloruro de benzalconio
El medicamento contiene 0,1 mg de cloruro de benzalconio por mililitro (0,1 mg/ml).
El cloruro de benzalconio puede ser absorbido por las lentes de contacto blandas y cambiar su color. Debe retirar las lentes de contacto antes de administrar las gotas y esperar al menos 15 minutos antes de volver a colocarlas.
El cloruro de benzalconio también puede causar irritación ocular, especialmente en personas con síndrome de ojo seco o trastornos de la córnea (la capa transparente del frente del ojo). Si experimenta sensaciones anormales en el ojo, picazón o dolor en el ojo después de usar el medicamento, debe consultar a un médico.
3. Cómo usar Tobradex
Este medicamento debe usarse siempre según las indicaciones de su médico. En caso de dudas, debe consultar a su médico o farmacéutico.
La dosis de Tobradex se determina individualmente para cada paciente por su médico. El médico determinará cuánto tiempo debe usar el medicamento. Si el médico no indica lo contrario, debe administrar 1 o 2 gotas del medicamento en el saco conjuntival (entre el ojo y la parte inferior del párpado) del ojo infectado, cada 4-6 horas.
Uso en niños
El medicamento puede usarse en niños mayores de 2 años en las mismas dosis que en adultos.
La seguridad y eficacia en niños menores de 2 años no han sido establecidas y no hay datos disponibles sobre el uso en este grupo de edad.
Uso en pacientes con trastornos hepáticos o renales
No se ha estudiado el efecto de Tobradex en estas poblaciones de pacientes. Sin embargo, debido a la baja absorción sistémica de tobramicina y dexametasona después de su administración tópica, se considera que no es necesario modificar la dosis.
Tobradex está indicado únicamentepara administración en los ojos.
1
2
3
4
- 1. Preparar el frasco de Tobradex y un espejo.
- 2. Lavar las manos.
- 3. Agitar el frasco.
- 4. Retirar la tapa. Si después de retirar la tapa, el anillo de seguridad está suelto, debe desecharlo antes de usar el medicamento.
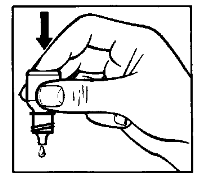
- 5. Tomar el frasco con la mano y dirigirlo hacia arriba con la parte inferior, sosteniéndolo con el pulgar y el dedo medio (dibujo 1).
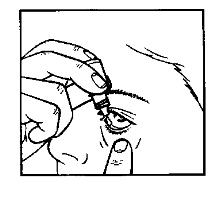
- 6. Inclinar la cabeza hacia atrás. Levantar el párpado inferior hacia abajo con un dedo limpio para formar una "bolsa" entre el párpado y el globo ocular; la gota debe caer en esta bolsa (dibujo 2).
- 7. Acercar la punta del gotero al ojo. Para facilitar la administración, puede usar un espejo.
- 8.
No tocar la punta del gotero con el ojo, el párpado, la zona alrededor del ojo ni otras superficies.
No seguir esta recomendación puede causar infección de las gotas. El uso de gotas infectadas puede llevar a complicaciones peligrosas e incluso a la pérdida de la visión.
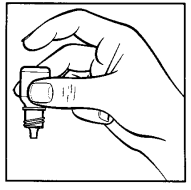
- 9. Presionar suavemente la parte inferior del frasco para hacer que salga una sola gota de Tobradex (dibujo 3). Si la gota no cae en el ojo, debe repetir el intento.
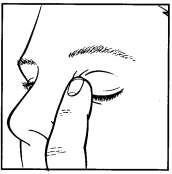
- 10. Después de administrar Tobradex, soltar el párpado inferior. Cerrar suavemente el ojo y presionar el ángulo del ojo cerca de la nariz con el dedo (dibujo 4). Esto ayuda a prevenir que el medicamento se absorba en todo el cuerpo.
- 11. Si es necesario administrar el medicamento en ambos ojos, debe repetir los pasos anteriores para el segundo ojo.
- 12. Inmediatamente después de usar el medicamento, cerrar el frasco.
- 13. Debe usar un solo frasco de Tobradex a la vez.
Uso de una dosis mayor de la recomendada de Tobradex
En caso de sobredosis, el exceso de medicamento se puede enjuagar con agua tibia. No debe administrar una dosis adicional. La próxima dosis se debe administrar a la hora habitual.
Olvido de una dosis de Tobradex
Si el paciente olvida administrar una dosis de Tobradex, debe continuar con el tratamiento y administrar la próxima dosis según el esquema de dosificación. Si falta poco tiempo para la próxima dosis, debe omitir la dosis olvidada y continuar con el esquema de dosificación prescrito. No debe administrar una dosis doblepara compensar la dosis olvidada.
En caso de dudas adicionales sobre el uso de este medicamento, debe consultar a un médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, Tobradex puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Si el paciente experimenta reacciones alérgicas, incluyendo erupciones cutáneas, hinchazón de la cara, los labios, la lengua y (o)
la garganta, lo que puede causar dificultades para respirar o tragar, o experimenta otros efectos adversos graves,
debe suspender el uso de Tobradex y consultar inmediatamente a un médico o acudir a la sala de emergencias del hospital más cercano.
Durante el uso de Tobradex, se han observado los siguientes efectos adversos:
No muy frecuentes(pueden ocurrir en menos de 1 de cada 100 pacientes): presión intraocular elevada, dolor en el ojo, picazón en el ojo, sensación de incomodidad en el ojo, irritación en el ojo.
Raros(pueden ocurrir en menos de 1 de cada 1.000 pacientes): inflamación de la córnea, alergia ocular, visión borrosa, síndrome de ojo seco, enrojecimiento, trastornos del gusto.
Frecuencia desconocida(la frecuencia no puede determinarse a partir de los datos disponibles): hinchazón de los párpados, enrojecimiento de los párpados, dilatación de la pupila, aumento de la lágrima, visión borrosa, reacciones alérgicas graves (hipersensibilidad), mareos, dolor de cabeza, náuseas, sensación de incomodidad en el estómago, reacciones cutáneas graves (eritema multiforme), picazón, hinchazón de la cara, aumento del crecimiento del vello en el cuerpo (especialmente en mujeres), debilidad muscular y pérdida de masa muscular, estrías púrpuras en la piel, aumento de la presión arterial, menstruación irregular o ausencia de menstruación, cambios en la cantidad de proteínas y calcio en el organismo, supresión del crecimiento en niños y adolescentes, así como hinchazón y aumento de peso, visible especialmente en el tronco y la cara (enfermedad conocida como síndrome de Cushing) (véase el punto 2 "Advertencias y precauciones").
Notificación de efectos adversos
Si se producen efectos adversos, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad, Consumo y Bienestar Social,
Calle de Alcalá, 56
28071 Madrid
Teléfono: 901 00 62 50
Fax: 913 33 48 50
Sitio web: https://www.aemps.gob.es/
Al notificar los efectos adversos, se puede recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Tobradex
Para evitar la contaminación del medicamento, el frasco debe desecharse después de 4 semanas desde la primera apertura. En el espacio indicado a continuación, debe anotar la fecha de apertura del frasco.
Fecha de primera apertura:…………….
Debe conservar el medicamento en un lugar donde no pueda ser visto ni alcanzado por los niños.
No debe conservar el medicamento a una temperatura superior a 25°C. No debe congelar.
Debe conservar el frasco en posición vertical.
Debe conservar el frasco bien cerrado.
No debe usar este medicamento después de la fecha de caducidad indicada en el embalaje después de: EXP.
La fecha de caducidad indica el último día del mes indicado.
El número de lote en el embalaje está indicado por "Lot".
No debe tirar los medicamentos por el desagüe ni por los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del embalaje y otra información
Qué contiene Tobradex?
- Los principios activos del medicamento son tobramicina 3 mg/ml y dexametasona 1 mg/ml.
- Los demás componentes son: cloruro de benzalconio, solución, edetato disódico, cloruro de sodio, sulfato de sodio anhidro, tiloxapol, hidroxietilcelulosa, agua purificada. Se agregan pequeñas cantidades de ácido sulfúrico y/o hidróxido de sodio (para ajustar el pH adecuado).
Cómo se presenta Tobradex y qué contiene el embalaje?
Tobradex es un líquido (suspensión), suministrado en un frasco de polietileno de 5 ml, con un gotero de polietileno y una tapa de polipropileno, en una caja de cartón.
Para obtener más información detallada, debe consultar al titular de la autorización de comercialización o al importador paralelo.
Título de la autorización de comercialización en Francia, país de exportación:
Novartis Pharma S.A.S
8-10, rue Henri Sainte-Claire Deville
92500 Rueil-Malmaison, Francia
Fabricante:
Alcon-Couvreur NV
Rijksweg 14
2870 Puurs, Bélgica
Siegfried El Masnou, S.A.
Camil Fabra 58
08320 El Masnou (Barcelona)
España
Novartis Farmacéutica, S.A.
Gran Vía de les Corts Catalanes, 764
08013 Barcelona
España
Novartis Pharma GmbH
Roonstrasse 25
90429 Núremberg
Alemania
Importador paralelo:
Medezin Sp. z o.o.
ul. Zbąszyńska 3, 91-342 Łódź
Reempaquetado por:
Medezin Sp. z o.o.
ul. Zbąszyńska 3, 91-342 Łódź
CEFEA Sp. z o.o. Sp. komandytowa
ul. Działkowa 56
02-234 Warszawa
Pharma Innovations Sp. z o.o.
ul. Jagiellońska 76
03-301 Warszawa
Laboratorium Galenowe Olsztyn Sp. z o.o.
ul. Spółdzielcza 25A
11-001 Dywity
Synoptis Industrial Sp. z o.o.
ul. Szosa Bydgoska 58
87-100 Toruń
Número de autorización de comercialización en Francia, país de exportación:
34009 344 299 7 2
344 299-7
Número de autorización de importación paralela: 404/19
Fecha de aprobación de la hoja de instrucciones: 25.09.2024
[Información sobre la marca registrada]
- País de registro
- Principio activo
- Requiere recetaSí
- Titular de la autorización de comercialización (TAC, MAH)Novartis Pharma S.A.S.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a TobradexForma farmacéutica: Gotas, (3 mg + 1 mg)/mlPrincipio activo: dexamethasone and antiinfectivesFabricante: Rafarm S.A.Requiere recetaForma farmacéutica: Gotas, (5 mg + 1 mg)/mlPrincipio activo: dexamethasone and antiinfectivesFabricante: Dr. Gerhard Mann Chem. - Pharm. Fabrik GmbHRequiere recetaForma farmacéutica: Ungüento, (5 mg + 0.3 mg)/gPrincipio activo: dexamethasone and antiinfectivesFabricante: Dr. Gerhard Mann Chem. - Pharm. Fabrik GmbHRequiere receta
Alternativas a Tobradex en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Tobradex en Україна
Alternativa a Tobradex en Іспанія
Médicos online para Tobradex
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Tobradex – sujeta a valoración médica y normativa local.














