
Mirtagen
Consulta con un médico sobre la receta médica de Mirtagen

Cómo usar Mirtagen
Hoja de instrucciones del paquete: información para el usuario
Atención: Debe conservar la hoja de instrucciones. La información en el embalaje primario está en un idioma extranjero.
Mirtagen (Mirtazapina SmeltTab Mylan 45 mg)
45 mg, tabletas que se disuelven en la boca
Mirtazapina
Mirtagen y Mirtazapina SmeltTab Mylan 45 mg son nombres comerciales diferentes del mismo medicamento.
Es importante leer atentamente el contenido de la hoja de instrucciones antes de tomar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a un médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para una persona. No debe dárselo a otros. El medicamento puede dañar a otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos todos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Mirtagen y para qué se utiliza
- 2. Información importante antes de tomar Mirtagen
- 3. Cómo tomar Mirtagen
- 4. Posibles efectos adversos
- 5. Cómo conservar Mirtagen
- 6. Contenido del paquete y otra información
1. Qué es Mirtagen y para qué se utiliza
Mirtagen pertenece a un grupo de medicamentos llamados antidepresivos.
Mirtagen se utiliza para tratar la depresión en adultos.
2. Información importante antes de tomar Mirtagen
Cuándo no tomar Mirtagen:
- si el paciente es alérgico a la mirtazapina o a cualquiera de los demás componentes de este medicamento (enumerados en el punto 6),
- si actualmente o recientemente (en las últimas 2 semanas) se han tomado medicamentos de la clase de los inhibidores de la monoaminooxidasa (IMAO).
Advertencias y precauciones
Cuándo no tomar Mirtagen o consultar a un médico antes de iniciar su uso:
Si el paciente ha experimentado algún síntoma como erupción cutánea grave o descamación, ampollas y (o) úlceras en la mucosa de la boca
después de tomar Mirtagen o otros medicamentos.
Se han notificado reacciones cutáneas graves durante el tratamiento con Mirtagen, como el síndrome de Stevens-Johnson, la necrolisis tóxica epidermal y la reacción medicamentosa con eosinofilia y síntomas generales. Si se observa alguno de los síntomas descritos en el punto 4 con respecto a las reacciones cutáneas graves, debe interrumpir el tratamiento y acudir urgentemente a un médico. Si el paciente ha experimentado reacciones cutáneas graves, no debe reiniciar el tratamiento con Mirtagen.
Niños y adolescentes
Mirtagen no debe administrarse a niños y adolescentes menores de 18 años, ya que no se ha establecido su eficacia. También se debe destacar que, en el caso de la ingesta de medicamentos de este grupo, los pacientes menores de 18 años están expuestos a un mayor riesgo de efectos adversos, como intentos de suicidio, pensamientos suicidas y hostilidad (especialmente agresión, comportamiento rebelde y manifestaciones de ira). Sin embargo, el médico puede recetar Mirtagen a pacientes menores de 18 años, considerando que está en su mejor interés. Si el médico ha recetado Mirtagen a un paciente menor de 18 años y el paciente desea discutirlo, debe volver a consultar a su médico. En caso de que se desarrollen o empeoren los síntomas mencionados anteriormente en pacientes menores de 18 años que toman Mirtagen, debe informar a su médico. Además, no se ha demostrado el impacto a largo plazo de Mirtagen en la seguridad relacionada con el crecimiento, la maduración y el desarrollo cognitivo y del comportamiento en este grupo de edad. Se ha observado con más frecuencia un aumento significativo de peso en pacientes tratados con mirtazapina en este grupo de edad en comparación con los adultos.
Pensamientos suicidas y empeoramiento de la depresión y los trastornos de ansiedad
Los pacientes con depresión pueden tener pensamientos de autolesión o pensamientos suicidas. Estos pensamientos pueden aumentar cuando se inician los medicamentos antidepresivos, ya que estos medicamentos actúan lentamente, generalmente en unos 2 semanas o más.
Esto puede ocurrir:
- Si el paciente ha tenido previamente pensamientos de autolesión o suicidio.
- Si el paciente es un adulto joven. La información de los estudios clínicos ha mostrado un mayor riesgo de comportamiento suicida en adultos con trastornos psiquiátricos tratados con medicamentos antidepresivos menores de 25 años.
En caso de que surjan pensamientos de autolesión o pensamientos suicidas, debe comunicarse de inmediato con un médico o acudir urgentemente al hospital.
Puede ser útil hablar con alguien cercano de la familia o un amigo. El paciente puede informar a estas personas sobre su depresión y pedirles que lean esta hoja de instrucciones para que puedan decirle si notan un empeoramiento de su estado de salud o cambios inusuales en su comportamiento.
Antes de iniciar el tratamiento con Mirtagen, debe discutir con su médico o farmacéutico si tiene o ha tenido alguna de las siguientes enfermedades:
- convulsiones(epilepsia)
- enfermedades hepáticas, incluyendo ictericia
- enfermedades renales
- enfermedades cardíacas o antecedentes de enfermedades cardíacas en la familia, incluyendo ciertos trastornos cardíacos que pueden causar cambios en el ritmo cardíaco, infarto de miocardio reciente, insuficiencia cardíaca o el uso de ciertos medicamentos que pueden alterar el ritmo cardíaco
- hipotensión
- esquizofrenia
- trastornos afectivos bipolares(períodos alternados de estado de ánimo elevado y depresión)
- diabetes(puede ser necesario ajustar la dosis de insulina o otros medicamentos hipoglucémicos)
- enfermedades oculares, como el glaucoma
- dificultades para orinar, que pueden deberse a una próstata agrandada.
Pacientes ancianos
- Los pacientes ancianos suelen ser más sensibles, especialmente a los efectos adversos de los medicamentos antidepresivos.
Durante el tratamiento
Debe informar a su médico:
- en caso de que aparezcan síntomas de infección como fiebre alta, dolor de garganta, úlceras en la boca. En casos raros, estos síntomas pueden ser indicativos de
trastornos en la producción de glóbulos sanguíneos por la médula ósea. Aunque son raros, estos síntomas suelen aparecer después de 4-6 semanas de tratamiento.
Mirtagen y otros medicamentos
No debe tomar Mirtagen al mismo tiempo que:
- inhibidores de la monoaminooxidasa(IMAO) ni antes de que transcurran dos semanas desde que dejó de tomarlos. Tampoco debe iniciar el tratamiento con Mirtagen antes de que transcurran dos semanas desde que dejó de tomar inhibidores de la MAO. Ejemplos de inhibidores de la MAO son: moklobemida, tranylcipromina (medicamentos antidepresivos) y selegilina (utilizada en el tratamiento de la enfermedad de Parkinson).
Debe decirle a su médico o farmacéutico sobre todos los medicamentos que está tomando actualmente o recientemente, así como sobre los medicamentos que planea tomar, incluyendo los medicamentos de venta libre, y especialmente sobre:
- otros medicamentos antidepresivos como los ISRS(por ejemplo, citalopram), venlafaxina, L-triptófano o triptanes(utilizados en el tratamiento de la migraña), tramadol(medicamento analgésico), linezolida(antibiótico), sales de litio(utilizadas en el tratamiento de ciertos trastornos psiquiátricos) y preparados que contienen hierva de San Juan(preparados herbales utilizados en el tratamiento de la depresión). En casos muy raros, en pacientes que toman solo Mirtagen o en terapia combinada con estos medicamentos, puede ocurrir un síndrome serotoninérgico. Algunos de sus síntomas son fiebre, sudoración, aumento de la frecuencia cardíaca, diarrea, (movimientos musculares no controlados) espasmos musculares, escalofríos, aumento de los reflejos, ansiedad, cambios de humor, pérdida de conciencia. Debe comunicarse de inmediato con un médico si ocurren varios de estos síntomas juntos.
- medicamentos utilizados en el tratamiento de ansiedad y insomniocomo las benzodiazepinas, por ejemplo, diazepam, clordiazepóxido.
- medicamentos utilizados en el tratamiento de esquizofreniacomo olanzapina.
- medicamentos utilizados en el tratamiento de alergiascomo cetirizina.
- medicamentos utilizados en el tratamiento de dolor intensocomo morfina. Mirtagen en combinación con estos medicamentos puede aumentar la somnolencia inducida por estos medicamentos.
Medicamentos que aumentan la cantidad de mirtazapina en la sangre:
- medicamentos utilizados en el tratamiento de infecciones; medicamentos antibacterianos (como eritromicina), medicamentos antifúngicos (como ketconazol), medicamentos utilizados en el tratamiento de infecciones por VIH y SIDA (como inhibidores de la proteasa del VIH, por ejemplo, ritonavir, nelfinavir); medicamentos antidepresivos(como nefazodona) y medicamentos utilizados en el tratamiento de úlceras gástricas (como cimetidina). En combinación con Mirtagen, estos medicamentos pueden aumentar la concentración de mirtazapina en la sangre. Debe informar a su médico sobre la ingesta de estos medicamentos. Puede ser necesario reducir la dosis de Mirtagen, y después de terminar el tratamiento con estos medicamentos, aumentar la dosis de Mirtagen.
Medicamentos que disminuyen la cantidad de mirtazapina en la sangre:
- carbamazepina y fenitoína, medicamentos utilizados en el tratamiento de la epilepsia; rifampicina, medicamento utilizado en el tratamiento de la tuberculosis .En combinación con Mirtagen, estos medicamentos pueden disminuir la concentración de Mirtagen en la sangre. Debe informar a su médico sobre la ingesta de estos medicamentos. Puede ser necesario aumentar la dosis de Mirtagen, y después de terminar el tratamiento con estos medicamentos, reducir la dosis de Mirtagen.
- warfarina, medicamento que previene la formación de coágulos. Mirtagen puede aumentar el efecto de la warfarina. Debe informar a su médico sobre la ingesta de estos medicamentos. En caso de tratamiento combinado con Mirtagen, se recomienda el monitoreo de la sangre.
Mirtagen y alcohol
En caso de beber alcohol mientras toma este medicamento, puede ocurrir somnolencia.
Es mejor evitar beber alcohol mientras toma Mirtagen.
Embarazo y lactancia
Experiencias limitadas con el uso de Mirtagen en mujeres embarazadas no muestran un aumento del riesgo. Sin embargo, se debe tener precaución durante el embarazo.
En caso de quedar embarazada o planificar un embarazo mientras toma Mirtagen, debe preguntar a su médico si puede continuar tomando el medicamento. Si Mirtagen se toma durante el embarazo o poco antes del parto, se recomienda la observación del recién nacido debido a la posible ocurrencia de efectos adversos.
Debe asegurarse de que la partera y (o) el médico sepan que está tomando Mirtagen.
El uso de medicamentos similares (ISRS) durante el embarazo puede aumentar el riesgo de un estado grave en los niños, llamado hipertensión pulmonar persistente del recién nacido (PPHN), que causa respiración acelerada y cianosis. Los síntomas suelen comenzar dentro de las 24 horas después del nacimiento del niño. En caso de que ocurran los síntomas descritos en el niño, debe comunicarse de inmediato con la partera o el médico.
Debe preguntar a su médico si puede amamantar mientras toma Mirtagen.
Si está embarazada o en período de lactancia, cree que puede estar embarazada o planea tener un hijo, debe consultar a su médico o farmacéutico antes de tomar este medicamento.
Conducción de vehículos y uso de máquinas
Mirtagen puede disminuir la alerta y la capacidad de concentración.
Antes de conducir vehículos o operar máquinas, debe asegurarse de que su capacidad de concentración y alerta no se hayan visto afectadas.
Mirtagen contiene aspartamo (E 951)
Este medicamento contiene 9 mg de aspartamo en cada tableta que se disuelve en la boca.
El aspartamo es una fuente de fenilalanina. Puede ser perjudicial para los pacientes con fenilcetonuria. Esta es una enfermedad genética rara en la que la fenilalanina se acumula en el cuerpo debido a su eliminación anormal.
3. Cómo tomar Mirtagen
Este medicamento debe tomarse siempre según las indicaciones de su médico o farmacéutico. En caso de dudas, debe consultar a su médico o farmacéutico.
Mirtagen está disponible en las siguientes dosis: 15 mg, 30 mg, 45 mg.
Dosificación
La dosis inicial recomendada es de 15 o 30 mg al día.Después de varios días de tratamiento, su médico puede recomendar aumentar la dosis a la más adecuada para usted (de 15 a 45 mg al día).
La dosis habitual se recomienda para pacientes de diferentes edades. Sin embargo, en personas de edad avanzada o con enfermedades renales y hepáticas, su médico puede recomendar una dosis diferente.
Cuándo tomar Mirtagen
Debe tomar Mirtagen todos los días a la misma hora.
Mirtagen se debe tomar preferiblemente en una sola dosis, antes de acostarse. Sin embargo, su médico puede recomendar tomar el medicamento en dos dosis divididas, una por la mañana y otra por la noche antes de acostarse. La dosis más alta debe tomarse antes de acostarse.
Información sobre la ingesta de tabletas que se disuelven en la boca:
Las tabletas deben tomarse por vía oral.
1. No debe partir la tableta que se disuelve en la boca
Para evitar partir la tableta que se disuelve en la boca, no debe presionar el bolsillo que contiene la tableta (Figura A).
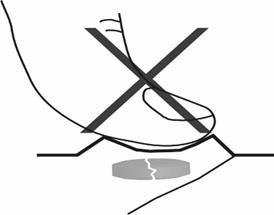
Figura A.
2. Debe separar el bolsillo con la tableta
Cada blister contiene 6 bolsillos con tabletas, separados por una línea perforada.
Debe doblar el blister y separar un bolsillo a lo largo de la línea perforada (Figura 1).
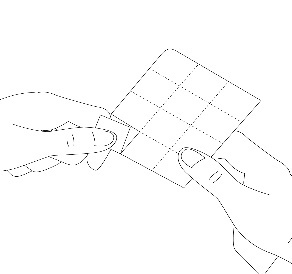
Figura 1.
3. Separe la película
Debe separar cuidadosamente la película que cubre, comenzando por una esquina (Figura 2).
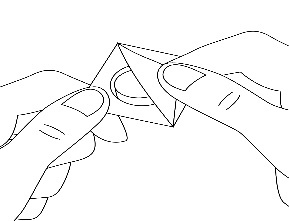
Figura 2.
4. Saque la tableta que se disuelve en la boca
Debe sacar la tableta que se disuelve en la boca con la mano seca y colocarla en la lengua. (Figura 3).
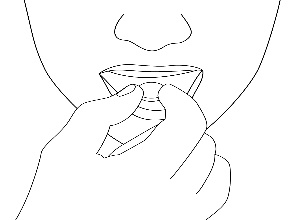
Figura 3.
La tableta se disuelve rápidamente y puede ser tragada sin necesidad de beber agua.
Cuándo puede esperar una mejora en su estado de ánimo
Mirtagen generalmente comienza a actuar después de 1 a 2 semanas, y después de 2 a 4 semanas, su estado de ánimo comenzará a mejorar.
Es importante discutir con su médico los efectos del medicamento durante las primeras semanas de tratamiento.
Después de 2 a 4 semanas desde el inicio del tratamiento con Mirtagen, debe discutir con su médico los progresos del tratamiento.
En caso de que no haya una respuesta clínica adecuada, su médico puede aumentar la dosis. Después de otras 2-4 semanas, debe discutir nuevamente con su médico los progresos del tratamiento. El tratamiento debe continuar hasta que los síntomas hayan desaparecido por completo, lo que generalmente dura de 4 a 6 meses.
Uso en niños y adolescentes menores de 18 años
Mirtagen no debe administrarse a niños y adolescentes menores de 18 años (véase el punto 2 "Niños y adolescentes").
Uso de una dosis mayor de la recomendada de Mirtagen
Si el paciente o alguien más ha tomado una dosis mayor de la recomendada de Mirtagen, debe comunicarse de inmediato con un médico.
Los signos más comunes de sobredosis de Mirtagen (sin otros medicamentos o alcohol) son somnolencia, desorientación, cambios en el ritmo cardíaco (taquicardia, ritmo cardíaco irregular) y (o) mareos.
Estos pueden ser síntomas de trastornos cardíacos potencialmente mortales llamados "torsades de pointes".
Olvido de una dosis de Mirtagen
En caso de que se olvide tomar una dosis de Mirtagen que debe tomarse una vez al día.
No debe tomar la dosis olvidada de Mirtagen, debe omitirla.
La siguiente dosis se debe tomar al día siguiente a la hora habitual.
No debe tomar una dosis doble para compensar la tableta olvidada.
En caso de que se olvide tomar una dosis de Mirtagen que debe tomarse dos veces al día.
En caso de que se olvide tomar la dosis matutina, debe tomarla junto con la dosis vespertina.
En caso de que se olvide tomar la dosis vespertina, no debe tomarla junto con la dosis matutina, debe omitirla y continuar el tratamiento tomando las dosis habituales por la mañana y por la noche.
En caso de que se olvide tomar ambas dosis, no debe intentar compensarlas, debe omitirlas. Al día siguiente, debe continuar el tratamiento tomando las dosis habituales por la mañana y por la noche.
Interrupción del tratamiento con Mirtagen
Debe dejar de tomar Mirtagen solo después de consultar a su médico.
No debe dejar de tomar el medicamento demasiado pronto, ya que esto puede causar una recaída en la enfermedad. Si hay una mejora, debe discutirla con su médico. Su médico le informará cuándo puede dejar de tomar el medicamento.
La interrupción repentina del tratamiento con Mirtagen puede causar náuseas, mareos, ansiedad o nerviosismo, dolor de cabeza. Se pueden evitar estos síntomas reduciendo gradualmente la dosis.
Su médico le informará cómo reducir gradualmente la dosis.
En caso de que tenga más dudas sobre el uso de este medicamento, debe consultar a su médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Si ocurre alguno de los siguientes síntomas, debe dejar de tomar Mirtagen y comunicarse de inmediato con un médico o acudir a la sala de emergencias del hospital más cercano:
Síntomas graves que requieren atención médica inmediata:
Raro(puede afectar a 1 de cada 1000 pacientes):
- pancreatitis, que causa dolor abdominal moderado a severo que se irradia hacia la espalda.
Frecuencia desconocida(la frecuencia de ocurrencia no puede determinarse a partir de los datos disponibles):
- convulsiones (epilepsia);
- icoloración amarilla de la piel o los ojos, que puede sugerir trastornos en la función hepática (ictericia);
- combinación de síntomas como fiebre de causa desconocida, sudoración, aumento de la frecuencia cardíaca, diarrea, (movimientos musculares no controlados) espasmos musculares, escalofríos, aumento de los reflejos, ansiedad, cambios de humor, pérdida de conciencia. En casos muy raros, pueden ser indicativos de un síndrome serotoninérgico;
- pensamientos de autolesión o suicidio o intentos de suicidio;
- erupciones cutáneas rojizas en el tronco en forma de placas redondas o manchas, a menudo con ampollas en la parte central; descamación de la piel; úlceras en la mucosa de la boca, garganta, nariz, ojos y genitales. Este tipo de erupciones cutáneas graves pueden estar precedidas por fiebre y síntomas similares a los de la gripe (síndrome de Stevens-Johnson, necrolisis tóxica epidermal)
- erupción generalizada, fiebre alta y aumento del tamaño de los ganglios linfáticos (síndrome DRESS, es decir, síndrome de sensibilidad a los medicamentos);
- síntomas de infección, como fiebre repentina, dolor de garganta, úlceras en la boca (agranulocitosis). La mirtazapina puede causar trastornos en la producción de glóbulos sanguíneos (supresión de la médula ósea). Algunas personas pueden volverse más propensas a las infecciones, ya que la mirtazapina puede causar una deficiencia temporal de glóbulos blancos (granulocitopenia). En casos raros, la mirtazapina también puede causar una deficiencia de glóbulos rojos y blancos, así como de plaquetas (anemia aplásica), deficiencia de plaquetas (trombocitopenia) o un aumento en el número de glóbulos blancos (eosinofilia);
- descomposición del tejido muscular, que causa dolor muscular, sensibilidad, rigidez y (o) debilidad, así como orina de color oscuro (rabdomiolisis);
- dificultades para orinar o vaciar la vejiga;
- niveles bajos de sodio en la sangre, que pueden causar sensaciones de debilidad y ser confundidos con dolor muscular. Esto puede deberse a una secreción inadecuada del hormona antidiurética, que causa una retención de agua en el cuerpo y una dilución de la sangre, reduciendo la cantidad de sodio.
Otros efectos adversos:
Muy frecuentes(pueden afectar a más de 1 de cada 10 pacientes):
- aumento del apetito o aumento de peso;
- somnolencia;
- dolor de cabeza;
- sequedad en la boca.
Frecuentes(pueden afectar a 1 de cada 10 pacientes):
- letargo;
- mareos;
- convulsiones o temblores;
- náuseas;
- diarrea;
- vómitos;
- estreñimiento;
- erupciones cutáneas o exantemas;
- dolores en las articulaciones, dolores musculares;
- dolores de espalda;
- mareos o desmayos al cambiar de posición repentinamente, por ejemplo, al levantarse (hipotensión ortostática);
- hinchazón (generalmente en los tobillos o los pies) debido a la acumulación de líquidos (edema);
- fatiga;
- sueños intensos;
- confusión;
- ansiedad;
- problemas para dormir.
Poco frecuentes(pueden afectar a 1 de cada 100 pacientes):
- sentimientos de excitación o euforia (mania);
- sensaciones cutáneas anormales, como ardor, picazón o entumecimiento (parestesia);
- síndrome de piernas inquietas;
- desmayos;
- sensaciones anormales en la boca (anestesia bucal);
- presión arterial baja;
- pesadillas;
- agitación;
- alucinaciones (ver, sentir o escuchar cosas que no existen);
- necesidad imperiosa de moverse.
Raros(pueden afectar a 1 de cada 1000 pacientes):
- temblores musculares o espasmos (convulsiones clónicas musculares);
- comportamiento agresivo;
- aumento de la actividad de las enzimas hepáticas en los análisis de sangre.
Frecuencia desconocida(la frecuencia de ocurrencia no puede determinarse a partir de los datos disponibles):
- sensaciones anormales en la boca, como ardor, picazón o entumecimiento (parestesia bucal);
- edema de la boca;
- niveles bajos de sodio en la sangre (hiponatremia) visibles en los análisis de sangre;
- aumento de la salivación;
- sonambulismo;
- dificultades para hablar;
- aumento del nivel de prolactina en la sangre (hiperprolactinemia, que incluye síntomas como el crecimiento de los senos y (o) secreción láctea del pezón).
Efectos adversos adicionales en niños y adolescentes
Los siguientes efectos adversos fueron observados con frecuencia en los estudios clínicos con niños menores de 18 años: urticaria y aumento de los triglicéridos en la sangre.
Notificación de efectos adversos
Si ocurren algún efecto adverso, incluidos todos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Salud
Al. Jerozolimskie 181C
02-222 Varsovia
tel.: +48 (22) 49 21 301
fax: +48 (22) 49 21 309
sitio web: https://smz.ezdrowie.gov.pl
Al notificar los efectos adversos, se pueden recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Mirtagen
Debe conservar el medicamento en un lugar donde no pueda ser visto ni alcanzado por los niños.
No debe tomar este medicamento después de la fecha de caducidad impresa en el paquete.
La fecha de caducidad es el último día del mes indicado.
No hay instrucciones especiales para el almacenamiento.
No debe tirar los medicamentos por el desagüe ni a los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Mirtagen?
- El principio activo de Mirtagen es la mirtazapina. Cada tableta que se disuelve en la boca contiene 45 mg de mirtazapina.
- Los demás componentes son: crospovidona, manitol (E 421), celulosa microcristalina, aspartamo (E 951) (véase el punto 2 "Mirtagen contiene aspartamo (E 951) y manitol (E 421)"), aroma a fresa y guaraná, aroma a menta, dióxido de silicio y estearato de magnesio.
Cómo se presenta Mirtagen y qué contiene el paquete?
Tabletas redondas, blancas, con la letra "A" grabada en una cara y "38" en la otra.
Tamaños de paquete: 30 tabletas que se disuelven en la boca.
Para obtener más información, debe consultar al titular de la autorización de comercialización o al importador paralelo.
Titular de la autorización de comercialización en Holanda, país de exportación:
Mylan Pharmaceuticals Ltd, Damastown Industrial Park, Mulhuddart, Dublin 15, Dublín, Irlanda
Fabricante:
Gerard Laboratories, 35/36 Baldoyle Industrial Estate, Grange Road, Dublín 13, Irlanda
Mylan Hungary Kft., Mylan utca 1, H-2900 Komárom, Hungría
Importador paralelo:
Delfarma Sp. z o.o., ul. Św. Teresy od Dzieciątka Jezus 111, 91-222 Łódź
Reempaquetado por:
Delfarma Sp. z o.o., ul. Św. Teresy od Dzieciątka Jezus 111, 91-222 Łódź
Número de autorización en Holanda, país de exportación: RVG 34054
Número de autorización de importación paralela: 306/22
Fecha de aprobación de la hoja de instrucciones: 23.11.2023
[Información sobre la marca registrada.]
- País de registro
- Principio activo
- Requiere recetaSí
- Titular de la autorización de comercialización (TAC, MAH)Mylan Pharmaceuticals Ltd
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a MirtagenForma farmacéutica: Comprimidos, 15 mgPrincipio activo: mirtazapinaRequiere recetaForma farmacéutica: Comprimidos, 30 mgPrincipio activo: mirtazapinaRequiere recetaForma farmacéutica: Comprimidos, 45 mgPrincipio activo: mirtazapinaRequiere receta
Alternativas a Mirtagen en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Mirtagen en Испания
Alternativa a Mirtagen en Украина
Médicos online para Mirtagen
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Mirtagen – sujeta a valoración médica y normativa local.









